
 某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:分析 由图可知,从反应开始,A的物质的量减少,B的物质的量增加,则A为反应物、B为生成物,开始至4min时,A减少0.8mol-0.4mol=0.4mol,B增加0.4mol-0.2mol=0.2mol,第8min时A、B的物质的量不再变化,达到平衡状态,以此来解答.
解答 解:(1)由图可知,从反应开始,A的物质的量减少,B的物质的量增加,则A为反应物、B为生成物,开始至4min时,A减少0.8mol-0.4mol=0.4mol,B增加0.4mol-0.2mol=0.2mol,由反应速率之比等于化学计量数之比可知,A、B的化学计量数比为2:1,且后来达到平衡状态,则反应为2A?B,
故答案为:2A?B;
(2)降低温度,正逆反应速率都减慢,故答案为:减慢;减慢;
(3)第4min时,A的物质的量仍在减少,为正反应阶段,正、逆反应速率的大小关系为:v(正)>v(逆),故答案为:>;
(4)A.恒温恒容充入He使压强增大,参加反应的气体的浓度不变,在反应速率不变,故A错误;
B.缩小体积,使压强增大,参加反应气体的浓度增大,故B正确;
C.恒温恒压充入He,体积增大,参加反应气体的浓度减小,反应速率减小,故C错误;
D.平衡后加入催化剂,反应速率增大,故D正确.
故答案为:BD.
点评 本题考查物质的量随时间变化曲线,为高频考点,把握图象中物质的量的变化、平衡状态的判断、速率比较等为解答的关键,侧重分析与应用能力的考查,注意速率的比较,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若降低温度,可以加快反应速率 | |
| B. | 增大O2浓度可以增大反应速率 | |
| C. | 随着反应的进行,正反应速率逐渐减小,最后变为0 | |
| D. | 达到化学平衡状态时,SO2和SO3的浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种定香剂,以芳香醇A为原料合成H的一种流程如下:
)是一种定香剂,以芳香醇A为原料合成H的一种流程如下:
 (R1、R表示氢原子或烃基)
(R1、R表示氢原子或烃基) ;E的官能团名称是碳碳双键、羧基.
;E的官能团名称是碳碳双键、羧基. .
. 、
、 .
. (其他试剂自选).
(其他试剂自选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数.B原子核内质子数和中子数相等.下列叙述不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数.B原子核内质子数和中子数相等.下列叙述不正确的是( )| A. | C元素是非金属性最强的元素 | |
| B. | A元素最高价氧化物对应的水化物具有强氧化性 | |
| C. | 三种元素的原子半径的大小顺序是:B>C>A | |
| D. | B元素的氧化物、氢化物的水溶液都呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图.
一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题:
碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题: )等.
)等. 是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.
是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
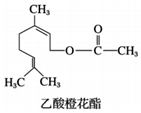 乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑥ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com