
���� ��1��NaHCO3���ȶ��������ֽ⣻
��2�������û����Ȼ�ͭ�еĽ���ͭ��
��3����������������Һ��Ӧ��Mg������������Һ����Ӧ��
��� �⣺��1��NaHCO3���ȶ��������ֽ⣬���ü��ȵķ������룬����ʽΪ���ʴ�Ϊ�����ȣ�2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O��
��2�������û����Ȼ�ͭ�еĽ���ͭ����ӦΪ��Cu2++Fe=Cu+Fe2+��Ȼ����˼��ɵõ��Ȼ��������ʴ�Ϊ��Fe��Cu2++Fe=Cu+Fe2+��
��3��Mg�������ǽ����������ᷴӦ������������������Һ��Ӧ��Mg������������Һ����Ӧ�����Կ���ѡȡ����������Һ�����Ӽ������ӷ���ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2�����ʴ�Ϊ��NaOH��Һ��2Al+2OH-+2H2O=2AlO2-+3H2����
���� ���⿼�����ʵķ��롢�ᴿ��������ѧ���ķ���������ʵ�����������������Ŀ��飬�ѶȲ���ע��������ʵ����ʵ���ͬ��ע�����ʱ���������µ����ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ˮ��Ӧ���ɼ���������Ʋ��Ǽ��������� | |
| B�� | ����FeCl3��Һ�е�����Fe2+��������KSCN��Һ | |
| C�� | SiO2���ܺ�����������Һ��Ӧ���ܺ�����ᷴӦ������������������ | |
| D�� | ��ͨ�����Ǵ��������ɿ���Na2O•CaO•6SiO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a��b��������ͬ�ֲ��ϵĵ缫 | |
| B�� | ��װ�ÿ�����ԭ��أ�Ҳ�����ǵ��� | |
| C�� | ��װ�ÿ�����ԭ��أ��������ҺΪϡ���� | |
| D�� | ��װ�õĵ缫������ͭп���������Һ��ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �Թ� | ���� | ���� |
| 1 | �����ˮ | ��Һ�����ɫ |
| 2 | ����������Һ��ˮԡ���� | δ�������� |
| 3 | �����ˮ | ��Һ�����ɫ |
| 4 | ����������Һ��ˮԡ���� | δ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�33.6 LSO3�к��з�ԭ�ӵ���ĿΪ1.5NA | |
| B�� | ��������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA | |
| C�� | 7.8 g Na2O2�к��е���������Ϊ0.2NA | |
| D�� | 1 molCl2�μӷ�Ӧת�Ƶ�����һ��Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
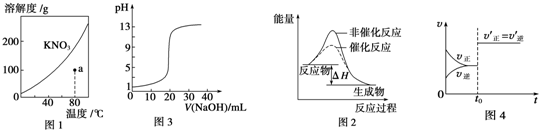
| A�� | ͼ1��ʾKNO3���ܽ�����ߣ�ͼ��a���Ӧ����Һ��80��ʱKNO3�ı�����Һ | |
| B�� | ͼ2��ʾij�����ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯 | |
| C�� | ͼ3��ʾ0.1000 mol•L-1 NaOH��Һ�ζ�20.00 mL 0.1000 mol•L-1������Һ�ĵζ����� | |
| D�� | ͼ4��ʾt0ʱ�ı����������������ѹǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
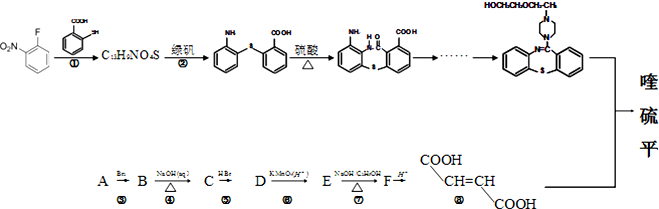
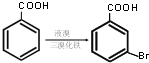 д���Լױ�Ϊԭ���Ʊ�
д���Լױ�Ϊԭ���Ʊ� �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com