
【题目】I.用序号按要求回答下列问题:
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是________;只存在离子键的是________;含有非极性键的离子化合物的是________。
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是________;仅破坏离子键的是________;仅破坏共价键的是________,既破坏离子键,又破坏共价键的是________。
(3)Na2O2的电子式为________________________,用电子式表示H2O的形成过程:________________________________________________。
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A______,B______,C______,D______,E______。
(2)B微粒的结构示意图为____________,C微粒的结构示意图为____________。
(3)A的单质与EB溶液反应的离子方程式为______________________________________。
【答案】⑥ ⑤ ④ ①③ ②⑤ ④ ⑥ ![]()
![]() Al Cl Mg2+ S2- H
Al Cl Mg2+ S2- H ![]()
![]() 2Al+6H+===2Al3++3H2↑
2Al+6H+===2Al3++3H2↑
【解析】
I.①H2O为只含共价键的共价化合物;②NH3为只含共价键的共价化合物;③KOH为既含离子键又含共价键的离子化合物;④Na2O2中既含钠离子和过氧根之间的离子键,又有氧原子之间的非极性共价键;⑤MgCl2为只含离子键的离子化合物;⑥Ne为不含化学键的稀有气体单质;
(2)①碘的升华为物理变化,只破坏分子间作用力;②NaCl固体溶于水发生电离破坏离子键;③O2溶于水只破坏分子间作用力④HCl气体溶于水发生电离破坏共价键⑤烧碱为离子晶体,熔化破坏离子键;⑥氯化铵受热分解生成氨气和HCl,所以氯离子和铵根之间的离子键被破坏,铵根内部的共价键被破坏;
Ⅱ. ①当A微粒失去3个电子后,其电子层结构与氖原子相同则A为Al;
②当B微粒得到1个电子后,其电子层结构与氩原子相同,则B为Cl;
③C微粒带两个单位正电荷,核电荷数为12,则C为Mg2+;
④D微粒有18个电子,当失去2个电子后显电中性,则D为S2-;
⑤E微粒不带电,原子核中只有一个质子,则E为H。
I.(1)不存在化学键的是稀有气体,即⑥Ne;只存在离子键的是⑤MgCl2;含有非极性键的离子化合物的是④Na2O2;
(2)根据分析可知化学键没有被破坏的是①③;仅破坏离子键的是②⑤;仅破坏共价键的是④;既破坏离子键,又破坏共价键的是⑥;
(3)过氧化钠由钠离子和过氧根组成,为离子化合物,所以电子式为![]() ;H2O为共价化合物,形成过程可以表示为
;H2O为共价化合物,形成过程可以表示为![]() ;
;
Ⅱ.(1)五种微粒分别为:Al、Cl、Mg2+、S2-、H;
(2)氯原子结构示意图为![]() ;Mg2+结构示意图为
;Mg2+结构示意图为![]() ;
;
(3)Al可以和HCl反应生成氯化铝和氢气,离子方程式为:2Al+6H+===2Al3++3H2↑。


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2+4H++4H2O= [Zn(H2O)4]2++4HOCH2CN,HOCH2CN的结构简式如下图所示,下列说法不正确的是
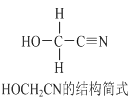
A. HOCH2CN分子中没有手性碳原子
B. 1mol HOCH2CN分子中含有σ键的物质的量为5mol
C. [Zn(CN)4]2-和[Zn(H2O)4]2+的中心原子配位数均为4
D. HOCH2CN分子中碳原子轨道的杂化类型分别是sp3和sp杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是

A. a电极是负极
B. b电极的电极反应为:4OH--4e-=2H2O+O2↑
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图(左)是还原铁粉与水蒸气反应的实验装置,实验时,B中灰色的铁粉变为黑色,且生成的黑色固体物质是一种可溶于稀盐酸的较复杂化合物。请回答下列问题:
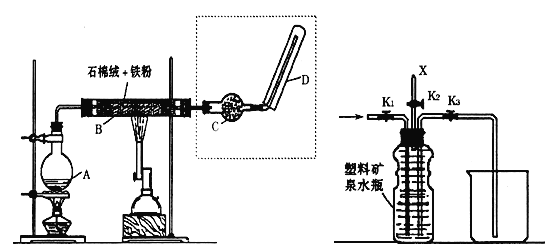
(1)B中发生反应的化学方程式为___________________
(2)反应前后A中投放碎瓷片的目的是________________________。
(3)某次实验后,取B中的固体物质少量,溶于足量稀盐酸,再滴加KSCN溶液。溶液颜色无明显变化,试解释原因__________________。
(4)上图(左)中虚线部分,可以用右图所示装置代替,在X口点燃收集到的气体即可检验H2的存在。实验开始时,打开K1、K2,关闭K3,使反应先进行一段时间之后,必须要进行______________操作,方可关闭K2、打开K3,再收集气体。当收集到半瓶气体时,停止加热,关闭K1,若要使H2顺利逸出而进行点燃实验,操作的方法是____________________。
(5)替代装置未像原装置那样使用干燥管,同样顺利完成了实验,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下进行甲、乙、丙三组实验:三组各取30.0 mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 255 | 385 | 459 |
产生气体体积/mL | 280 | 336 | 336 |
请回答:
(1)甲组实验中,盐酸______________(选填“适量”“过量”或“不足量”,下同),理由是______________。要算出盐酸的物质的量浓度,题中可作计算依据的数据是______________。求得的盐酸的物质的量浓度为______________。
(2)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是______________,求得的Mg、Al的物质的量之比为______________;
(3)在丙组实验之后,向容器中加入1.00 mol·L-1 NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶性固体,求滤液中各溶质的物质的量和所加入NaOH溶液的体积(写计算过程)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2H2O2(l)![]() 2H2O(l)+O2(g)能量变化如图所示,下列说法正确的是
2H2O(l)+O2(g)能量变化如图所示,下列说法正确的是
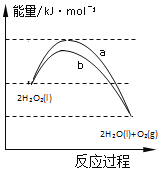
A. 由于分解反应,所以该反应吸热
B. 途径b改变了反应的热效应
C. 1 molH2O2(l)的能量高于1 molH2O(l)的能量
D. 途径a放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-中的几种,为确定其成分,完成了如下实验(已知:3NO3-+8Al+5OH-+2H2O ![]() 3NH3↑+ 8AlO2- )
3NH3↑+ 8AlO2- )
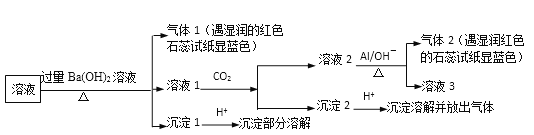
根据实验现象,所得结论错误的是
A.沉淀1加酸部分溶解,则含Mg2+和SO42-B.可能含Na+、Cl-
C.沉淀2加酸溶解,则含Al3+D.气体1遇水显碱性,则含NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
J | ||||
R |
(1)M的离子结构示意图为__________;元素T在周期表中位于第________族。
(2)J元素名称是______,他和氢组成10电子的化合物,其分子式为______________,属___________(填“离子化合物”或“共价化合物”)。
(3)R元素符号为_______,其最高能层符号是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2、CO、CO2和CH4都是中学化学常见的气体。某无色气体X可能含有上述4种气体中的一种或两种。为了确认气体X的组成,同学们按下图装置进行实验。(气体燃烧装置中能提供足量的氧气保证可燃性气体充分燃烧,甲烷燃烧的产物为CO2和H2O)
小资料:碱石灰的主要成分是CaO和NaOH,能吸收CO2和水蒸气。
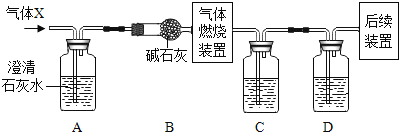
(1)装置A的作用是_________,装置B的作用是______。
(2)装置C盛放的试剂是_____(填序号),D中盛放的试剂是_____(填序号)。
a.烧碱溶液 b.浓硫酸
(3)若取1.6g气体X进行实验(假设每步反应都完全),发现装置A中无明显变化,装置C增重1.8 g,装置D增重2.2 g。通过计算回答:
①燃烧生成CO2______mol,H2O________mol;
②说明1.6g气体X中含有碳元素________g,含有氢元素_______g。是否含有氧元素?______(填“是”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com