
下列说法正确的是
A.参加反应物质的性质是决定化学反应速率的主要因素
B.化学反应速 率只能加快不能减慢
率只能加快不能减慢
C.决定化学反应速率的主要因素是浓度
D.增加反应物的用量一定能增大反应速率
科目:高中化学 来源:2016届广西桂林市高三第一次月考化学试卷(解析版) 题型:选择题
下列选用的相关仪器符合实验要求的是
A | B | C | D |
存放浓硝酸 | 分离水和乙酸乙酯 | 准确量取9.50 mL水 | 实验室制取乙烯 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2016届山东省新高三开学初模拟检测化学试卷(解析版) 题型:选择题
下列电离方程式中,错误的是
A.H2CO3  H++HCO3- ; HCO3-
H++HCO3- ; HCO3-  H++CO32-
H++CO32-
B.H2SO4 == 2H++SO42-
C.NaHS == Na++H++S2-
D.CH3COOH  H+ + CH3COO―
H+ + CH3COO―
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄石市高三9月调研考试化学试卷(解析版) 题型:填空题
(13分)节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若宁波全市的140余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2 CH3OH。请根据图示回答下列:
CH3OH。请根据图示回答下列:
(1)关于该反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
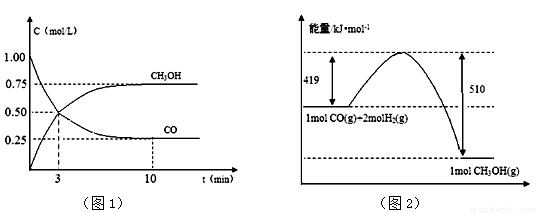
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,净测得CO和CH3OH(g)的浓度随时间变化如(图1)所示。从反应开始到平衡,CO的平均反应速率v(CO)= ,该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度 B.充入He气
C.再充入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量=_____g/mol。
(5)根据(图2),写出此反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是
A.pH=13 的溶液:Na+、NH4+、SO42-、Cl-
B.甲基橙呈黄色的溶液:Na+、K+、ClO-、AlO2-
C.0.1 mol/L 的KNO3 溶液:H+、Fe2+、Cl-、SO42-
D.水电离的c(H+)=1×10-13mol·L-1 的溶液中:K+、Ba2+、Br-、I-
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三7月月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下述正确的是
A.58.5g氯化钠晶体中含有NA个氯化钠分子
B.20g重水(D2O)中含有的电子数为10NA
C.标准状况下,22.4LCCl4含有NA个CCl4分子
D.120gNaHSO4晶体中阳离子和阴离子的总数为3NA
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期第一次质检化学试卷(解析版) 题型:实验题
(12分)实验室有NH4HCO3和NaHSO3的混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。(已知酸性KMnO4被SO2还原的反应原理:SO2+MnO4-+H2O→SO42-+Mn2++H+)回答以下问题:
(1)化学小组主要选用了下列药品和仪器进行实验。(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)

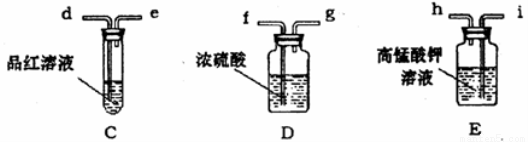
请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b…)
a→ →_______→______→______→f→g→_______→_______。
(2)实验开始,混合物加酸前,A装置需要鼓入空气,作用是_____________;加酸后A装置再次鼓入空气的作用是 。
(3)E装置的作用是 。
(4)实验中若C瓶中溶液褪色,则测定结果可能会偏__________。(填高或低)
(5)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为______。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:填空题
(共12分)氯元素是生产生活中常见的非金属元素。
(1)将Cl2通入NaOH溶液中得到以NaClO为有效成分的漂白液,写出该反应的离子方程式 ;不直接用Cl2作漂白剂的原因是 (写出两条)。
(2)使用Cl2为自来水消毒时,会与水中的有机物生成对人体有害的有机氯化物。下列物质中可以替代Cl2为自来水杀菌消毒的是 (填字母序号)。
a.臭氧 b.NH3 c.明矾 d.ClO2
(3)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是 和 。
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是 。
③已知:2H2O2(l)=2H2O(l)+O2(g) ΔH1 = -196.46 kJ·mol-1
H2(g)+1/2O2(g)= H2O(l) ΔH2 = -285.84 kJ·mol-1
Cl2(g)+H2(g)=2HCl(g) ΔH3 = -184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三第一次月考化学试卷(解析版) 题型:填空题
(8分)(原创)铜及其化合物在工农业生产中都有着广泛应用。
(1)火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2=Cu2S+2FeS+SO2、Cu2S+O2=2Cu+SO2。当有1molCu生成,则第一个反应中转移电子 mol。
(2)某种处理火法炼铜中SO2废气的工艺流程如下图所示。
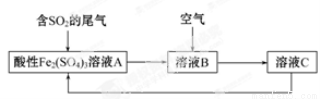
①溶液A中发生的反应为 。
②由流程图可推知Fe3+、O2、SO42-的氧化性由强到弱的顺序为 。
(3)已知反应:3Cu+2NO3-+xH+=3Cu2++2R+yH2O。则
①反应中的x= 。
②反应产物R的化学式为 。
③参加反应的Cu和消耗的HNO3物质的量之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com