
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是:
Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是:
A.充电时阳极反应:Ni(OH)2 — e—+ OH—== NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH—向正极移动
科目:高中化学 来源: 题型:
营养平衡、合理用药是保证人体健康和生活质量的重要途径。
(1)人体需要的营养素主要有糖类、 、蛋白质、无机盐、维生素和水。人们每天摄取的热能中大约有75%来自糖类,淀粉是一种重要的多糖,它在人体内水解的最终产物是 (填分子式)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 (填试剂名称)共同完成。
(2)下列物质中,具有解热镇痛疗效的是 (填字母,下同),治疗胃酸过多的是 。
a.氨基酸 b.阿司匹林 c.青霉素 d.复方氢氧化铝
(3)在食品加工或餐饮业中,特别要严加控制用量的物质是 (填字母)。
a.氯化钠 b.碳酸氢钠 c.亚硝酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物丙由如下反应得到:C4H10O C4H8 C4H8Br2
甲 乙 丙
丙的结构简式不可能是:
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是:( )
A.充电时作阳极,放电时作正极 B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时放正极
查看答案和解析>>
科目:高中化学 来源: 题型:
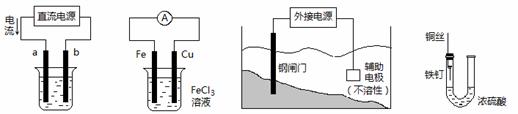
关于下列各装置图的叙述中,不正确的是:( )
① ② ③ ④
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
I、有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请回答问题。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中除稀有气体外电负性最小的元素 |
(1)B原子最外层共有 种不同运动状态的电子,
(2)C的第一电离能比F 的 (填“大”或“小”),
(3)D与E可形成 DE3分子,其 中心原子的杂化方式为 ,其空间构型为 。
II、原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满。下表是主要化合价及原子半径数据:
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3 +5 | -2 +6 | -1 +7 | +2 | +1 +2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
 (1)B、C、D三种元素第一电离能数值由小到大的顺序是 (填元素符号);
(1)B、C、D三种元素第一电离能数值由小到大的顺序是 (填元素符号);
(2)F2+与NH3 形成配离子时提供空轨道的为 (填写微粒的化学式);往某种蓝色溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成深蓝色透明溶液,可得到含有上述配离子的配合物。写出沉淀溶解的离子方程式 。
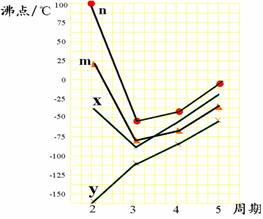
(3)图中四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,请选出字母C所对应元素的氢化物所在的折线 (填n、m、x或y)。
查看答案和解析>>
科目:高中化学 来源: 题型:
对化学反应:A(g) + 3B(g)===2C(g) +2D(g)来说,下列四种不同情况下的反应速率最快的是( )
A.υ(A)= 0.005mol/(L·s)
B.υ(B)= 0.6 mol/(L·min)
C.υ(C)= 0.5 mol/(L·min)
D.υ(D)= 0.45 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
中学常见的某反应的化学方程式为:
A + B → C + D +H2O(未配平,且反应条件略去)。
请回答下列有关问题。
(1)若A是铜,B是稀硝酸(过量),则此反应的离子方程式为:
。
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,某探究性学习小组利用下图中所列装置设计实验,证明上述反应中有C、D生成。
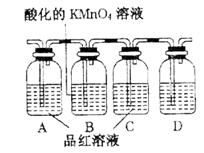
则①B瓶溶液的作用是:
C瓶溶液的作用是:
②若不使用C瓶溶液,只使用B瓶溶液,也可以达到原来B、C瓶所起的作用,此时B瓶溶液中的实验现象应为: 。
(3)若C是无色有刺激性气味的气体,其水溶液呈弱碱性。写出C发生催化氧化反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,固定体积为2 L密闭容器中,发生反应:2SO2(g)+O2(g)2SO3(g) ΔH<0,n(SO2)随时间的变化如表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是( )
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com