
 .
.分析 (1)根据C、H元素守恒确定烃A的实验式,可知该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为(CH3)3C-CH=CH2;
(2)根据烷烃2,5-二甲基己烷的碳架,在该烷烃的碳架上添上碳碳三键即可;
(3)烃1mol与2mol HCl完全加成,则该烃分子有2个双键或1个三键,1mol氯代烷能和4mol氯气发生完全取代反应,则氯代烷分子中有4个H原子,所以原烃分子中有2个H原子;
(4)根据乙烯的结构知,要使化学式为C6H12的某烯烃的所有碳原子都在同一平面上,用甲基代替乙烯中的H原子即可,从而确定该烯烃的结构简式.
解答 解:(1)根据C、H原子守恒可知,烃A中C、H原子数目之比=1.2mol:1.2mol×2=1:2,故烃A的实验式为CH2;n(烃A):n(C):n(H)=n(烃A):n(CO2):2n(H2O)=0.2mol:1.2mol:1.2mol×2=1:6:12,即1个分子中含有6个C原子、12个H原子,故该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2.2-二甲基丁烷,则该烃的结构简式为:(CH3)3C-CH=CH2,故答案为:(CH3)3C-CH=CH2;
(2)2,5-二甲基己烷的碳架为:C-C(C)-C-C-C(C)-C,在该碳架上添加碳碳三键,可以得到炔烃,该炔烃的结构简式为: ,故答案为:
,故答案为: ;
;
(3)烃1mol与2mol HCl完全加成,则该烃分子有2个双键或1个三键,1mol氯代烷能和4mol氯气发生完全取代反应,则氯代烷分子中有4个H原子,氯代烷分子中有2个H原子是烃与氯化氢加成引入的,所以原烃分子中有2个H原子,故该烃为CH≡CH,
故答案为:CH≡CH;
(4)根据乙烯的结构知,要使化学式为C6H12的某烯烃的所有碳原子都在同一平面上,用甲基代替乙烯中的H原子即可,则该烯烃的结构简式为(CH3)2C=C(CH3)2,
故答案为:(CH3)2C=C(CH3)2.
点评 本题考查有机物推断,为高频考点,侧重考查学生的分析能力,注意把握有机物结构简式的书写,明确有机物结构是解本题关键,会根据通式、物质结构进行推断,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验结论 |
| ①氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C生成的速率与C分解的速率相等 | |
| B. | 单位时间内生成a mol A,同时生成2a mol B | |
| C. | 容器内各组分的总质量不再变化 | |
| D. | 混合气体的总物质的量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

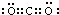 、
、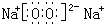 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com