
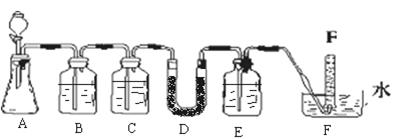
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | | 除去CO2中的水蒸气 |
| E | | |
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | | 除去CO2中的HCl |
| C | 浓硫酸 | |
| E | NaOH溶液 | 除去O2中的CO2 |


科目:高中化学 来源:不详 题型:问答题

| 物质 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 293K溶解度(g) | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
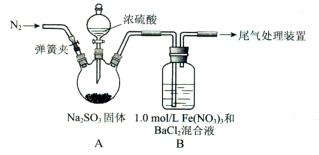
 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。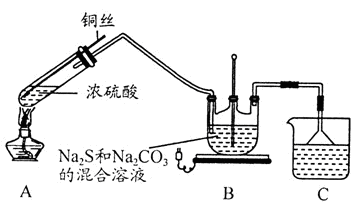
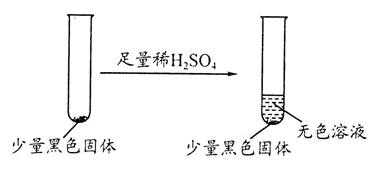

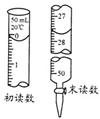
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.加热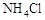 晶体时,将湿润的红色石蕊试纸靠近试管口,检验 晶体时,将湿润的红色石蕊试纸靠近试管口,检验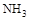 的生成 的生成 |
B.向某溶液中加入足量盐酸酸化,无现象,再加人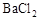 溶液,有白色沉淀生成,说明原溶液中存在 溶液,有白色沉淀生成,说明原溶液中存在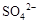 |
| C.酸碱中和滴定实验中用到的玻璃仪器仅有酸式滴定管、碱式滴定管和烧杯 |
D.用量筒量取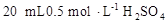 溶液于烧杯中,加水80mL,,配制成0.1 溶液于烧杯中,加水80mL,,配制成0.1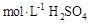 溶液 溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
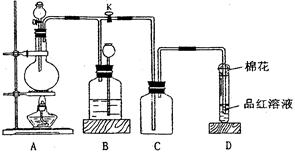
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

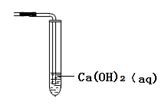
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
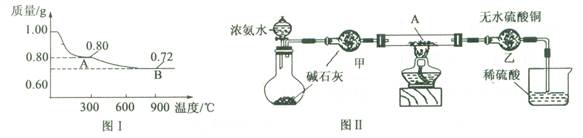
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com