
��Ũ������H3AsO3��SnCl2�����ӷ���ʽΪ��3SnCl2��12Cl����6 H����2H3AsO3=== 2As ��3SnCl62����6M�����ڸ÷�Ӧ��˵������ȷ�������
����������H3AsO3 �ڻ�ԭ�ԣ�Cl����As �� ÿ����1mol As����Ӧ��ת�Ƶ� �ӵ����ʵ���Ϊ3 mol �� MΪOH�� �� SnCl62������������
�ӵ����ʵ���Ϊ3 mol �� MΪOH�� �� SnCl62������������
A���٢ۢ� B���٢ڢܢ� C���٢ڢۢ� D��ֻ�Т٢�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ӻ�ˮ�п��Ի�õ�ˮ��ʳ�Σ�������ȡþ��������ʡ�
��һ����ˮ�����ķ�����Ҫ�� ��ֻ��һ�֣���
�������Ӻ�ˮ����ȡ���þ����������ͼ��ʾ��
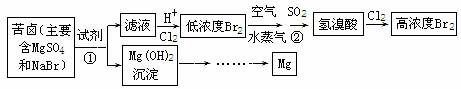
��1����ȡBr2 ʱ����һ��ͨ��Cl2 ������Ӧ�����ӷ���ʽ��
����SO2���� �����������ԭ�����ԣ�
�ڶ���ͨ��Cl2 ��Ҫ��ȡBr2 ��Ҫ���еIJ���Ϊ ��
��2��Ϊ��ʵ�ֶ�þ���ӵĸ��������м���������Լ��� ���ѧʽ����
��ӽ�Լ��Դ����߽���þ�Ĵ��ȷ��������������˵�ұ���ķ�����
������ĸ����
A. Mg(OH)2 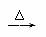 MgO
MgO 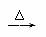 Mg
Mg
B. Mg(OH)2  MgO
MgO 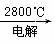 Mg
Mg
C. Mg(OH)2  ��ˮMgCl2
��ˮMgCl2 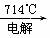 Mg
Mg
D. Mg(OH)2 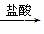 MgCl2����Һ��
MgCl2����Һ�� Mg
Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£�10 mL 0.40 mol/L H2O2��Һ�������ֽ⣬��ͬʱ�̲������O2�������������Ϊ��״�������±���
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
������������ȷ���ǣ���Һ����仯���Բ��ƣ�
A��0~6 min��ƽ�ⷴӦ���ʣ�v(H2O2)��3.3��10��2 mol/(L��min)
B��6~10 min��ƽ�ⷴӦ���ʣ�v(H2O2)��3.3��10��2 mol/(L��min)
C����Ӧ��6 minʱ��c(H2O2)=0.30 mol/L
D����Ӧ��6 minʱ��H2O2�ֽ���50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ��N2(g)+3H2(g)
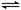 2NH3(g)��һ�ֹ�ҵ�ϳɰ��������ϳ����صĵļ�������ͼ���£�
2NH3(g)��һ�ֹ�ҵ�ϳɰ��������ϳ����صĵļ�������ͼ���£�
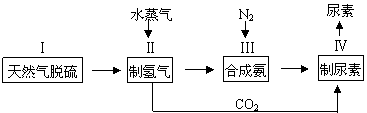 |
(1)����II��������ԭ�����£�
CH4(g)��H2O(g)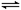 CO(g)��3H2(g) CO(g)��H2O(g)
CO(g)��3H2(g) CO(g)��H2O(g)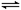 CO2(g)��H2(g)
CO2(g)��H2(g)
���������У��������Ϸ�Ӧ���ܼӿ췴Ӧ���ʵ��� ��
a. �����¶� b. ����He c. ������� d. ����ѹǿ
(2)��Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽΪ
��
(3)CO2��H2�ڸ��¡���ѹ�����������¿ɺϳ�CH3CH2OH����Ӧ�Ļ�ѧ����ʽ
_________________________________����CH3CH2OH������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���Ȼ�ϵ�أ��õ���и����ϵĵ缫��Ӧʽ�ǣ�_________________________��
 (4)��֪���صĽṹ��ʽΪH2N��
(4)��֪���صĽṹ��ʽΪH2N��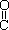 ��NH2����д�����ص�ͬ���칹���к������Ӽ��Ļ�ѧʽ ��
��NH2����д�����ص�ͬ���칹���к������Ӽ��Ļ�ѧʽ ��
(5)��֪CO2�� 2NH3 CO(NH2)2 �� H2O�����ϳ����ص�������ת����Ϊ80%ʱ��100�ּ���Ϊԭ���ܹ��ϳ� �����ء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����
A��ԭ�ӵĵ��Ӳ���Խ�࣬ԭ�Ӱ뾶Խ��
B��ͬ��Ԫ������ԭ����������Ϊ16��26��36��46
C����A�����A��Ԫ�ؼ���γɹ��ۻ���������ӻ�����
D��±��Ԫ�صĵ��ʾ��������ԣ�������۶��ǣ�7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���Ԫ������ �ڱ���λ�õ�������ȷ����
�ڱ���λ�õ�������ȷ����
A��ԭ�ӵ��������2�����ӵ�Ԫ��һ���Ǣ�A��Ԫ��
B��Ԫ�����ڵ���������������������֮��Ϊ1��Ԫ�ض��ǽ���Ԫ��
C������˹ר���״κϳ���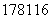 Xԭ�ӣ�116��Ԫ��λ��Ԫ�����ڱ��е������ڢ�A��
Xԭ�ӣ�116��Ԫ��λ��Ԫ�����ڱ��е������ڢ�A��
D��ԭ����������������3(С��8)��Ԫ��һ���Ƿǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ľṹ��ʽ��ͼ������˵����ȷ����
A�����������ܷ���������Ӧ�Ĺ�������2��
B��1 mol��������� 4 mol NaOH�����кͷ�Ӧ
4 mol NaOH�����кͷ�Ӧ
C��1 mol����������������Na��Ӧ��������1.5 mol H2
D����������O2��Cu�����������ȵ������£��ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���������ǣ� ��
A��һ���ˮ����10�����ϵ�ˮ���Ӿ۽����һ��ˮ�����ţ��д������ˮ����ѧ���ܰѴ������ˮ���5-8��ˮ������ɵ�С������ˮ��һ������125 mL��ά������6Сʱ������ˮ�������ת����̸ı���ˮ���Ӽ�Ľṹ����������
B�����ӻ������п����й��ۼ�
C����ѧ������ظ�ԭ���������Ȼ�ĵ�����BN�����и��۵㡢���ܶȡ���Ӳ�ȵ����ԣ�����������ԭ�Ӿ���
D���á�˺�ѡ������ɴ�ʯī�����а�����ĵ���̼ԭ������ϣ�ʯīϩ���������ַ�����C60�����ʯ��̼ԭ���л�á�ֻ��һ��̼ԭ�Ӻ��̼��Ƭ��Ҳ����Ϊ�о�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ���� ��������
A��2013��1��1������ʡ��ʽ����������������ָ����AQI��������PM2.5��PM10��O3��CO2��SO2��NO2��6��ָ��
B���˴Ź����ǡ���������ǡ������ǵȶ��������л�������ṹ�ķ���
C��ʯ���ѽ⡢��ˮ��þ�������绯����ά���ƻ��ȹ����ж�������ѧ�仯
D��������������ʳ�������������������������ʳ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com