
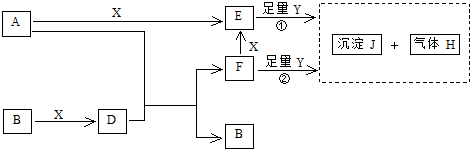
已知:A是略带甜味气体,可作为果实的催熟剂。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
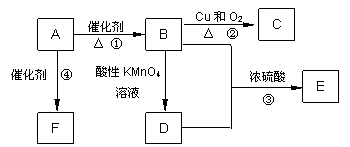
(1)A的结构式为__________,E的名称为__________。(2分)
(2)B分子中的官能团名称是_________,请设计一种验证B物质存在该官能团的方法____________________________________________。(2分)
(3)写出下列反应的化学方程式并指出反应类型:(4分)
①_______________________________________;反应类型是_____________;
④______________________ ____________;反应类型是__________.
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:阅读理解
| ② | |||
| ⑦ | ⑧ |

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ② | |||
| ⑦ | ⑧ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
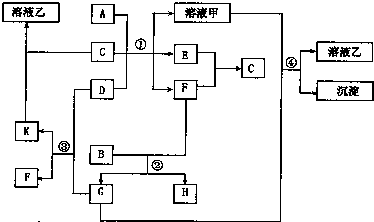


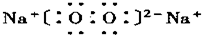
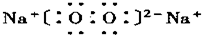
查看答案和解析>>
科目:高中化学 来源: 题型:
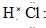
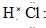
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com