
向各盛有1L水的甲、乙、丙、丁四个烧杯内分别加入等物质的量的Na、Na2O、Na2O2和NaOH,固体完全溶解后,各烧杯中溶质的质量分数大小顺序是()
| A. | 甲<乙<丙<丁 | B. | 丁<甲<乙=丙 | C. | 甲=丁<乙=丙 | D. | 丁<甲<丙<乙 |
| 钠的重要化合物;化学方程式的有关计算. | |
| 专题: | 计算题;元素及其化合物. |
| 分析: | 先根据钠原子守恒计算溶质的质量,再根据反应方程式计算溶液的质量,从而计算溶液的质量分数,涉及到的化学方程式有Na+H2O=NaOH+ |
| 解答: | 解:钠、氧化钠、过氧化钠和水反应的方程式分别如下: Na+H2O=NaOH+ Na2O+H2O=2NaOH,溶液增加的质量=m(Na2O)=0.1mol×62g/mol=6.2g; Na2O2+H2O=2NaOH+ 将氢氧化钠加入水中,溶液增加的质量为氢氧化钠的质量=0.1mol×40g/mol=4g; 所以溶液增加的质量大小顺序为:钠<氢氧化钠<氧化钠=过氧化钠, 根据钠原子守恒知,0.1mol的钠、氧化钠、过氧化钠、氢氧化钠溶于水所得氢氧化钠的物质的量分别为:0.1mol 通过以上分析可知,0.1mol的钠、氧化钠、过氧化钠、氢氧化钠分别溶于水所得溶液的质量分数分别为:
故选B. |
| 点评: | 本题以钠及其化合物的性质考查了溶液质量分数大小的比较,难度较大,明确溶液质量增加的量是解本题的关键. |


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.按系统命名法,化合物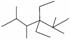 的名称是2,3,5,5四甲基4,4二乙基己烷
的名称是2,3,5,5四甲基4,4二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段为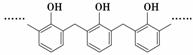 的高聚物,其单体是甲醛和苯酚
的高聚物,其单体是甲醛和苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
对于合成氨反应,达到平衡后,以下分析正确的是( )
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeC l3 高效,且腐蚀性小。请回答下列问题:
l3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+
|
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |

 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
 xFe3++yH2O
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
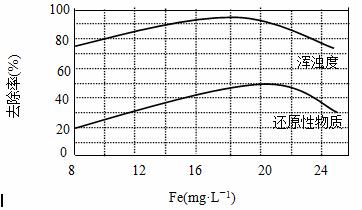
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的叙述中 ,正确的是
,正确的是 ()
()
| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属与水 | |
| C. | 碱金属在空气中加热均可生成多种氧化物 | |
| D. | 碱金属的硬度小、密度小、熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
(1)H2(g)+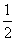 O2(g)===H2O(g) ΔH1=a kJ·mol-1
O2(g)===H2O(g) ΔH1=a kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1
(3)H2(g)+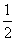 O2(g)===H2O(l) ΔH3=c kJ·mol-1
O2(g)===H2O(l) ΔH3=c kJ·mol-1
(4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ·mol-1
下列关系式中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示。下列有关黄曲霉毒素M1的说法正确的是( )
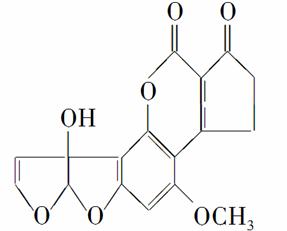
A.黄曲霉毒素M1的分子式为C17H14O7
B.黄曲霉毒素M1含有羟基,此羟基能被催化氧化为醛基
C.1 mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2 mol NaOH
D.1 mol黄曲霉毒素M1最多能 与7 mol H2发生加成反应
与7 mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com