
【题目】某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如图所示. 
(1)通过上述实验过程,一定不存在的离子是 .
(2)反应①中生成A的离子方程式为 .
(3)若测得X溶液中c(H+)=5mol/L,则X溶液中(填“含”或“不含”)Fe3+ , c(Fe3+)=mol/L(若填不含,则不需计算),X溶液中c(Cl﹣)=mol/L.
【答案】
(1)CO32﹣、SO32﹣、NO3﹣
(2)3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O
(3)含;1;14.5
【解析】解:在强酸性溶液中一定不会存在CO32﹣和SO32﹣离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42﹣离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2 , E为HNO3 , 说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3 , 说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3 , H为NaAlO2 , 沉淀G为Fe(OH)3 , 说明溶液中含有Al3+离子,计算氢氧化铁物质的量和元溶液中亚铁离子物质的量判断原溶液中含有Fe3+ , 溶液中含有Fe2+离子,就一定不含NO3﹣离子,结合溶液中阴阳离子电荷守恒计算确定是否含有的离子Cl﹣ , (1)由以上分析可知一定不存在CO32﹣、SO32﹣、NO3﹣ , 所以答案是:CO32﹣、SO32﹣、NO3﹣;(2)①Fe2+离子被氧化为Fe3+离子,反应的离子方程式为:3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O,所以答案是:3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O;(3)A是NO物质的量= ![]() =0.01mol,F为NH3物质的量=
=0.01mol,F为NH3物质的量= ![]() =0.015mol,I为氢氧化铝沉淀物质的量=
=0.015mol,I为氢氧化铝沉淀物质的量= ![]() =0.01mol,10mL X溶液中n(H+)=5mol/L×0.01L=0.05mol,根据反应3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O,可知Fe2+物质的量为0.03mol;,G为氢氧化铁物质的量=
=0.01mol,10mL X溶液中n(H+)=5mol/L×0.01L=0.05mol,根据反应3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O,可知Fe2+物质的量为0.03mol;,G为氢氧化铁物质的量= ![]() =0.04mol,原溶液中含铁离子物质的量n(Fe3+)=0.01mol,c(Fe3+)=
=0.04mol,原溶液中含铁离子物质的量n(Fe3+)=0.01mol,c(Fe3+)= ![]() =1mol/L,溶液中正电荷为:n(Fe3+)+2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=0.01×3+2×0.03mol+3×0.01mol+0.015mol+0.05mol=0.185mol;沉淀C为硫酸钡,其物质的量=
=1mol/L,溶液中正电荷为:n(Fe3+)+2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=0.01×3+2×0.03mol+3×0.01mol+0.015mol+0.05mol=0.185mol;沉淀C为硫酸钡,其物质的量= ![]() =0.02mol,n(SO42﹣)=0.02mol,硫酸根离子所带的负电荷为:0.02mol×2=0.04mol,电荷守恒可知含有Cl﹣ , n(Cl﹣)=0.185mol﹣0.04mol=0.145mol,得到溶液中氯离子浓度c(Cl﹣)=
=0.02mol,n(SO42﹣)=0.02mol,硫酸根离子所带的负电荷为:0.02mol×2=0.04mol,电荷守恒可知含有Cl﹣ , n(Cl﹣)=0.185mol﹣0.04mol=0.145mol,得到溶液中氯离子浓度c(Cl﹣)= ![]() =14.5mol/L,
=14.5mol/L,
所以答案是:含;1;14.5.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】已知破坏1molH-H键、Cl-Cl键、H-Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与Cl2生成1 molHCl总的过程需要( )
A. 放热185kJB. 吸热185kJC. 放热92.5 kJD. 吸热92.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的多种化合物在工业中有重要的应用.
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性.
①Na2S2O4中S元素的化合价为 .
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为(填化学式).
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2 . 该反应的化学方程式为 .
(2)铬会造成环境污染.某酸性废水中含有Cr2O72﹣ , 处理时可用焦亚硫酸钠(Na2S2O3)将Cr2O转化为毒性较低的Cr3+ , 再调节pH至8,使铬元索沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg/L,达到排放标准.
①Na2S2O3参加反应的离子方程式为 .
②处理后的废水中Cr3+的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来.
请回答下列问题:
(1)维生素A中的含有官能团种类有 , (官能团名称),它使溴水褪色(填“能”或“否”),
(2)维生素A1的结构简式如图,若1mol维生素A1分子最多可跟molH2发生加成反应. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面4组物质中,能发生反应且既属于离子反应又属于氧化还原反应的是( )
A. 硫酸钠溶液与氯化钡溶液 B. 铝片与硝酸汞溶液
C. 稀硫酸与铜片 D. 硝酸钠溶液与氯化钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 电子云通常是用小黑点来表示电子的多少
B. 1s22s12p1表示原子的激发态
C. s-s σ键与s-p σ键的电子云形状相同
D. 电子仅在激发态跃迁到基态时才会产生原子光谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 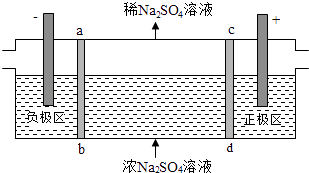
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~F六种有机物的相互转化关系如图所示:
已知:① 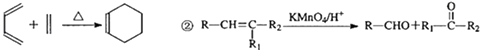
③X的产量可以用来衡量一个国家石油化工发展水平,N是X最简单的同系物.
据此回答下列问题:
(1)A的核磁共振氢谱有4个峰,峰面积比3:1:2:2,且A和N可发生反应①,则A的结构简式为 , A与Br2按物质的量比1:1发生加成反应,请写出生成的所有产物的结构简式为(不考虑顺反异构).
(2)M与足量的氢气加成后的产物P的一氯代物只有3种,请用系统命名法给P命名,P的名称为
(3)E→F的反应类型为 , 化学方程式为 .
(4)E在浓硫酸存在下能生成多种化合物,写出符合下列条件的有机物的结构简式.含有六元环:含有三元环: .
(5)现有另一种有机物G,已知G与E无论按何种比例混合,只要总质量一定,完全燃烧时生成的CO2、H2O以及消耗的O2均为定值.请写出两种符合下列要求的G的结构简式、 .
①M(G)<M (E);
②G的核磁共振氢谱有两个峰,且峰面积比为1:3.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com