
����Ŀ��A��B��D��E��G��ԭ������������������ֶ�����Ԫ�أ�A��Eͬ���壬A��B��E��ԭ������������֮��Ϊ19��B��G�ĵ��ʶ�����H2��Ӧ������HX��(X����B��G)���⻯��,DΪͬ��������Ԫ����ԭ�Ӱ뾶����Ԫ�ء�
(1)B��Ԫ�����ڱ��е�λ����______��
(2)D�����ֳ����������о�����____________(�������Ӽ����������ۼ���)��
(3)E������������Ӧˮ�����Ũ��Һ��ľ̿����,��Ӧ�Ļ�ѧ����ʽΪ____________��
(4)D������������Ӧˮ�������Һ��G�ĵ��ʷ�Ӧ,��Ӧ�����ӷ���ʽΪ___________��
(5)��ԭ�ӽṹ������B��G���ʶ�����H2��Ӧ����HX���⻯������ԭ��________��
���𰸡���2���ڵ�VIIA�� ���Ӽ� 2H2SO4(Ũ)+C ![]() CO2��+2SO2��+2H2O Cl2+2OH���TClO��+Cl��+H2O ������ͬ��VIIA��,��ԭ��������������Ϊ7,��������ԭ�ӹ���һ�Ե����γɹ��ۼ�
CO2��+2SO2��+2H2O Cl2+2OH���TClO��+Cl��+H2O ������ͬ��VIIA��,��ԭ��������������Ϊ7,��������ԭ�ӹ���һ�Ե����γɹ��ۼ�
��������
A��B��D��E��G ��ԭ������������������ֶ�����Ԫ�أ�����B��Gͬ���壬B ��G �ĵ��ʶ�����H2��Ӧ������HX��(X����B��G)���⻯���BΪFԪ�أ�GΪClԪ�أ�DΪͬ��������Ԫ����ԭ�Ӱ뾶����Ԫ�أ�ԭ����������F��С��Cl����DΪNaԪ�أ�A��Eͬ���壬A��B��E��ԭ������������֮��Ϊ19����֪A��E��������������Ϊ6����AΪOԪ�أ�EΪSԪ�أ���϶�Ӧ���ʡ�������������Լ�Ԫ��������֪ʶ�Ľ��
A��B��D��E��G ��ԭ������������������ֶ�����Ԫ�أ�����B��Gͬ���壬B ��G �ĵ��ʶ�����H2��Ӧ������HX��(X����B��G)���⻯���BΪFԪ�أ�GΪClԪ�أ�DΪͬ��������Ԫ����ԭ�Ӱ뾶����Ԫ�أ�ԭ����������F��С��Cl����DΪNaԪ�أ�A��Eͬ���壬A��B��E��ԭ������������֮��Ϊ19����֪A��E��������������Ϊ6����AΪOԪ�أ�EΪSԪ�أ�
(1)BΪFԪ�أ�λ�����ڱ���2���ڵ�VIIA�壻
(2)DΪNaԪ�أ������ֳ���������Ϊ�����ơ��������ƣ����߾��������Ӽ���
(3)E������������Ӧˮ�����Ũ��ҺΪŨ���ᣬ����ǿ�����ԣ���ľ̿���ȷ�Ӧ��ѧ����ʽΪ2H2SO4(Ũ)+C![]() CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��
(4)�������������Ʒ�Ӧ�����Ȼ��ƺʹ������ƣ���Ӧ�����ӷ���ʽΪCl2+2OH-�TClO-+Cl-+H2O��
(5)������ͬ��VIIA�壬��ԭ��������������Ϊ7����������ԭ�ӹ���һ�Ե����γɹ��ۼ������ʶ�����H2 ��Ӧ����HX ���⻯�


 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��3�����ʽṹ������]
п�ڹ�ҵ������Ҫ���ã�Ҳ������������Ԫ�ء��ش��������⣺
��1��Znԭ�Ӻ�������Ų�ʽΪ________________��
��2����ͭ����������ʹ�õĺϽ�֮һ����Ҫ��Zn��Cu��ɡ���һ��������1��Zn��_______��1��Cu)(����ڡ���С�ڡ�)��ԭ����________________��
��3��ZnF2���нϸߵ��۵㣨872 ��)���仯ѧ��������_________��ZnF2�������л��ܼ���ZnCl2��ZnBr2��ZnI2�ܹ������Ҵ������ѵ��л��ܼ���ԭ����________________��
��4�����л����ݡ�����ҽ�伮�У�������¯��ʯ��ZnCO3����ҩ������������Ƥ����֢����洴�ˡ�ZnCO3�У������ӿռ乹��Ϊ________________��Cԭ�ӵ��ӻ���ʽΪ________________��
��5������Zn�����е�ԭ�Ӷѻ���ʽ��ͼ��ʾ�����ֶѻ���ʽ��Ϊ_______________���������ױ߱߳�Ϊa cm����Ϊc cm�������ӵ�������ֵΪNA��Zn���ܶ�Ϊ________________g��cm��3���г�����ʽ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij������Һ(���ܺ���Br����SO42-��H2SO3��NH4+)�ֱ��������ʵ�飺
�ټ���ʱ�ų����������ʹƷ����Һ��ɫ��
�ڼӼ�������Ժ���ʱ�ų����������ʹ��ʪ�ĺ�ɫʯ����ֽ������
�ۼ�����ˮʱ����Һ���Ի�ɫ���ټ���BaCl2��Һ�������İ�ɫ����������ϡ���ᡣ
�����������ʲ���ȷ������ԭ��Һ���Ƿ���ڵ���(����)
A.Br��
B.SO42-
C.H2SO3
D.NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������
��O2��O3 ��H2��D2��T2 ��12C��14C ��CH3CH2CH2CH3��(CH3)2CHCH3 ������Ͷ��� ��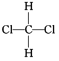 ��
��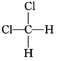 ��
��![]() ��
��![]() ����������ˮ ����Ͱ���
����������ˮ ����Ͱ���
��Ϊͬλ�ص���___(����ţ���ͬ)����Ϊͬ�����������___����Ϊͬϵ�����__����Ϊͬ���칹�����__������ͬһ���ʵ���__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����������ͽ��۾���ȷ����
ѡ�� | ʵ����� | ���� | ���� |
A | �����pH=2��HX��HY������ֱ�������������Ӧ������ˮ���ռ����� | HX�ų����������Ҳ�������H2��Ӧ���ʿ� | ���ǿ����HX��HY |
B | ��2 mL 0.1 mol/L Na2S��Һ�е�2��0.1 mol/L ZnSO4��Һ���ٵ�2��0.1 mol/L CuSO4 | �����ɰ�ɫ�����������ɺ�ɫ���� | �ܶȻ�(Ksp)��ZnS>CuS |
C | ��FeCl3��KSCN�����Һ�У���������KCl�Ĺ��� | ��Һ��ɫ��dz | FeCl3+3KSCN |
D | �����£���pH�Ʒֱ�ⶨ����NaA��Һ�ͱ���NaB��Һ��pH | pH��NaA��NaB | ���������ԣ�HA��HB |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ���ǣ� ��
A.�����������������������ֱ���ȫȼ�գ����߷ų���������
B.��C��ʯī����C�����ʯ����H=+1.9kJ��mol-1��֪�����ʯ��ʯī�ȶ�
C.��ϡ��Һ�У�H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ��mol-1��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ
D.��101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2H2O��l����H=-285.8kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������İ��������(NH2COONH4)�������Ƶ��ܱ����������(��������������䣬��������������Բ���)���ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4(s)![]() 2NH3(g)+CO2(g)��
2NH3(g)+CO2(g)��
��1�����в����жϸ÷ֽⷴӦ�Ѿ��ﵽ��ѧƽ��״̬����___(��ѡ��)��
A.2v��(NH3)=v��(CO2)
B.�ܱ������а��������ʵ�������
C.������CO2��NH3�����ʵ���֮�ȱ��ֲ���
D.�ܱ���������ѹǿ���ֲ���
E.�γ�6��N-H����ͬʱ��2��C=O������
��2����ʹ�÷�Ӧ�ķ�Ӧ�����������___(��ѡ��);
A.��ʱ�����CO2����
B.�ʵ������¶�
C.��������NH2COONH4(s)
D.ѡ���Ч����
��3����ͼ��ʾ��������Ӧ�жϿ���Ӧ���л�ѧ�����յ�����___�γ��������л�ѧ���ų�������(��д������������������С����)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڢ�CO2����NaCl����Na����Si����CS2�����ʯ���ߣ�NH4��2SO4�����Ҵ��У��ɼ��Լ��γɵķǼ��Է�����_______������ţ�����ͬ�������н������ӵ�������__�����Ӽ���γ������������________���������Ӿ������__������ԭ�Ӿ������__���١����������ʵ��۵��ɸߵ��͵�˳����__��
��2��A��B��C��DΪ���־��壬�������£�
A����̬ʱ�ܵ��磬����������
B��������CS2��������ˮ
C����̬ʱ�����磬Һ̬ʱ�ܵ��磬������ˮ
D����̬��Һ̬ʱ�������磬�۵�Ϊ3500 ��
���ƶ����ǵľ������ͣ�A��__��B��__��C��__��D��__��
��3����ͼ��A��D����ѧ��ѧ�̿����ϳ����ļ��־���ṹģ�ͣ�����д��Ӧ���ʵ����ƣ�A��__��B��__��C��__D��____��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E����Ԫ�أ����ǵ��������������ࡣ
��A�ĺ˵��������2�����γ��⻯��H2A�����⻯���ڳ�������Һ�壻
��A��B��Ԫ�ؿ��γ�B2A3������û������������ǿ�ᣬ��������ǿ�
��C+���ӱ�B3+���Ӷ�8�����ӣ�
��C��DԪ�ؿ����γɻ�����CD��
��CD����Һ��ͨ��������ӵ�����Һ����ɫ��
��E��Cͬ���壬��E��C���������Ӳ㣬E���ʿ�����ˮ��Ӧ��������.
�Իش�
��1��A��Ԫ�����ڱ��е�λ��___��B�����ӽṹʾ��ͼ___��������NH4D(��D-�����)�ĵ���ʽ___��
��2��C��ij�ּ������ӣ���ԭ�Ӻ��к�22�����ӣ��仯ѧ����Ϊ___��Ԫ��D����������ˮ���ﻯѧʽΪ___��
��3��B��C��E����Ԫ�صĽ���������ǿ������˳������ӦΪ��___����Ԫ�ط��ű�ʾ����
��4��д������B������������Һ��Ӧ�����ӷ���ʽ��___��
��5��д��E����ˮ��Ӧ�����ӷ���ʽ��___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com