
| A. | 150 mL 1 mol•L-1 NaCl溶液 | B. | 75 mL 2 mol•L-1 NH4Cl溶液 | ||
| C. | 150 L 3 mol•L-1 KCl溶液 | D. | 75 mL 1 mol•L-1 CaCl2溶液 |
分析 根据化学式可知1mol•L-1的AlCl3溶液中氯离子浓度为3mol/L,结合各选项中化学式判断溶液中氯离子浓度,注意离子的浓度与溶液的体积无关,与物质的构成有关.
解答 解:50mL 1mol•L-1AlCl3溶液中,氯离子的物质的量浓度为:1mol•L-1×3=3mol•L-1,
A.150 mL 1 mol•L-1NaCl溶液中,Cl-浓度为1mol•L-1×1=1mol•L-1,故A错误;
B.75 mL 2mol•L-1氯化铵溶液中,Cl-浓度为2mol•L-1×1=2mol•L-1,故B错误;
C.150 mL 3 mol•L-1KCl溶液中,Cl-浓度为3mol•L-1×1=3mol•L-1,故C正确;
D.75mL 1mol•L-1CaCl2溶液中,Cl-浓度为1mol•L-1×2=2mol•L-1,故D错误;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度较小,明确物质的构成是解答本题的关键,并注意离子的浓度与溶液的浓度的关系来解答即可.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
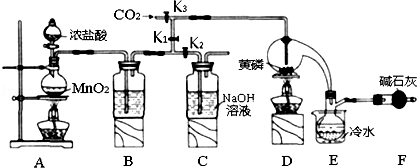
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF电离:HF(aq)?H+(aq)+F-(aq)△H=+10.4kJ/mol | |
| B. | 水解消耗0.1mol F-时,吸收的热量为6.77kJ | |
| C. | 中和热均为57.3 kJ/mol | |
| D. | 含0.1mol HF、0.1mol NaOH 的两种溶液混合后放出的热量为6.77kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质在酶的作用下水解的最终产物为氨基酸 | |
| B. | 向蛋白质溶液加入(NH4)2SO4浓溶液,会使其变性 | |
| C. | 天然蛋白质仅由碳、氢、氧、氮四种元素组成 | |
| D. | 氨基酸和蛋白质都是只能和碱反应的酸性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com