
| A. | 氯气 二氧化碳 氢氧化钠 | B. | 氯化钠 过氧化钠 氯化铵 | ||
| C. | 氯化钠 过氧化氢 氯化铵 | D. | 氯化钠 氦气 氢氧化钠 |
分析 活泼金属元素和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,据此分析解答.
解答 解:A.氯气为单质,只含共价键;二氧化碳为共价化合物,只含共价键;NaOH为离子化合物,含有离子键和共价键,故A错误;
B.NaCl为离子化合物,只含离子键;过氧化钠为离子化合物,含有离子键和共价键;氯化铵为离子化合物,含有离子键和共价键,故B错误;
C.NaCl为离子化合物,只含离子键;过氧化氢为共价化合物,只含共价键;氯化铵为离子化合物,含有离子键和共价键,故C正确;
D.NaCl为离子化合物,只含离子键;氦气为单原子分子,不含化学键;NaOH为离子化合物,含有离子键和共价键,故D错误;
故选C.
点评 本题考查化学键,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,注意稀有气体中不含化学键,为易错点.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:解答题
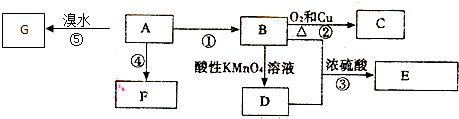
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
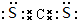 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) | B. | c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-) | ||
| C. | c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | D. | c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和乙烯:分别通入酸性KMnO4溶液 | |
| B. | 乙醇和乙酸:分别滴加NaOH溶液 | |
| C. | 苯和四氯化碳:分别与水混合、振荡、静置 | |
| D. | 棉花织品和羊毛织品:分别燃烧闻气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a≤100时,发生的离子反应为:OH-+H+=H2O | |
| B. | 当a≥300时,发生的离子反应为:OH-+3H++CO32-=2H2O+CO2↑ | |
| C. | 当100<a<200时,反应后的溶液中CO32-与HCO3-的物质的量之比为(a×10-4-0.01):(0.02-a×10-4) | |
| D. | 当a=200时,发生的离子反应为:OH-+2H++CO32-=H2O+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气和氯气光照爆炸得到HCl气体 | |
| B. | 在HCl合成塔,点燃的氢气中通入氯气产生HCl | |
| C. | 氯气在空气中点燃后通入氢气产生HCl | |
| D. | 点燃氢气和氯气混合气体产生HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
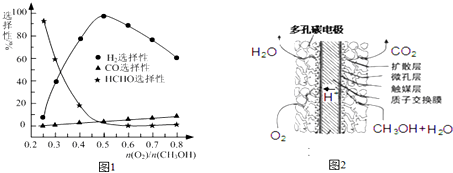
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 取少量溶液滴加Ca(OH)2溶液,观察是否出现白色浑浊,确定NaHCO3溶液中是否混有Na2CO3 | |
| B. | 苯酚沾到皮肤上,先用酒精清洗,再用水冲洗 | |
| C. | 将10g ZnSO4•7H2O溶解在90g水中,配制10%ZnSO4溶液 | |
| D. | 向稀硫酸中加几滴CuSO4溶液,可提高纯锌与稀硫酸的反应速率. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com