
分析 根据纯水中c(OH-)=c(H+),溶液显示中性进行分析;
根据该温度下纯水中氢离子浓度和氢氧根离子浓度,计算出水的离子积,
若温度不变,根据稀硫酸溶液中氢离子浓度和水的离子积计算出溶液中氢氧根离子的浓度,
若温度不变,依据氢氧化钠溶液中氢氧根离子浓度,结合离子积常数计算溶液中氢离子浓度.
解答 解:纯水显示中性,c(OH-)=c(H+)=5.0×10-7mol/L;
此温度下,水的离子积为:Kw=5.0×10-7×5.0×10-7=2.5×10-13,
若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,硫酸溶液中氢离子浓度c(H+)=5.0×10-3mol/L,c(OH-)=$\frac{2.5×10{\;}^{-13}}{5.0×10{\;}^{-3}}$mol/L=5.0×10-11 mol/L,
在该温度时,往水中滴入NaOH溶液,溶液中的c(OH-)=5.0×10-2mol/L,则溶液中c(H+)=$\frac{2.5×10{\;}^{-13}}{5.0×10{\;}^{-2}}$mol/L=5.0×10-12mol/L,
故答案为:5.0×10-7mol/L;5.0×10-11mol/L;5.0×10-12mol/L.
点评 本题考查了水的离子积常数的有关计算,注意水的离子积常数只与温度有关,与溶液的酸碱性无关,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | v(D)=6 mol•(L•min)-1 | B. | v(C)=0.5 mol•(L•s)-1 | ||
| C. | v(B)=0.6 mol•(L•s)-1 | D. | v(A)=0.15 mol•(L•s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| -c(NO)/mol•L -1 | 1.00×10 -3 | 4.50×10-4 | 2.50×10 -4 | 1.50×10 -4 | 1.00×10 -4 | 1.00×10 -4 |
| -c(CO)/mol•L-1 | 3.60×10 -3 | 3.05×10 -3 | 2.85×10 -3 | 2.75×10 -3 | 2.70×10 -3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学方程式为CO+H2O$?_{高温高压}^{催化剂}$CO2+H2 | |
| B. | 该反应的焓变为正值 | |
| C. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| D. | 升高温度,平衡右移,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2, | B. | O2 | C. | N2 | D. | CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2可用作呼吸面具的供氧剂 | |
| B. | 侯德榜“联合制碱法”制取的是碳酸钠 | |
| C. | 钠与乙醇反应,钠块沉入试管底部 | |
| D. | NaHCO3的热稳定性大于Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
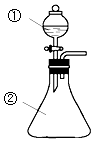 将①中液体逐滴滴入到②中(如图),实验结果与预测的现象一致的是( )
将①中液体逐滴滴入到②中(如图),实验结果与预测的现象一致的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氨水 | 氯化铝溶液 | 产生白色沉淀 |
| B | 浓硫酸 | 铜片 | 产生大量气体溶液变蓝 |
| C | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 |
| D | 稀盐酸 | Na2CO3与NaOH的混合液 | 立即产生大量气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是还原产物 | |
| B. | □处对应的物质为H2O | |
| C. | 氧化剂与还原剂物质的量之比为1:8 | |
| D. | 若1mol KMnO4参加反应,转移的电子的物质的量是4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com