
在密闭容器中发生如下反应:aX(g)+bY(g) cZ(g)+dW(g),反应达平衡后,W的浓度为0.5mol•L-1,保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为0.8mol•L-1。下列叙述不正确的是 ( )
A.平衡向逆反应方向移动 B.a+b > c+d
C.Z的体积分数减少 D.X的转化率减小
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
反应3A(g)+B(g)  2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.v (A)=0.15 mol·L-1·s-1 B.v (B)=0.3 mol·L-1·s-1
C.v (C)=0.5 mol·L-1·s-1 D.v (D)=0.4 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家刚刚发现的某种元素的一个原子,其质量是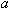 g,一个12C的原子质量是b g,
g,一个12C的原子质量是b g,
用NA是阿伏加德罗常数的值,下列叙述中不正确的是( )
A.该原子的摩尔质量是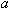 NA g·mol-1 B.Wg该原子中含有
NA g·mol-1 B.Wg该原子中含有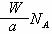 个原子
个原子
C.Wg该原子的物质的量是 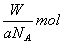 D.由已知信息可得:
D.由已知信息可得: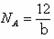 mol-1
mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,水的电离可达到平衡:H2O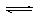 H++OH- △H>0,下列叙述正确的( )
H++OH- △H>0,下列叙述正确的( )
A. 向水中加入NaOH固体,平衡逆向移动,c(OH-)降低
B. 将水加热,Kw增大,c(OH-)不变
C. 向水中加入少量CH3COONa固体,平衡逆向移动。
D. 向水中加入少量稀硫酸,c(H+)增大,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂废水中含游离态氯,通过下列实验测定其浓度。①取水样10.0ml于锥形瓶中,加入10.0ml的K I溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。②取一滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol·L-1Na2S2O3溶液,调整液面,记下读数。③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+ 2Na2S4O6 试回答下列问答:
⑴步骤①加入的指示剂是 。
⑵步骤②应使用 式滴定管。
⑶判断达到滴定终点的实验现象是 ;
⑷氯的实际浓度比所测浓度会偏小,造成误差的原因是
(5)用0.1032mol/L HCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是
A、酸式滴定管未用标准盐酸溶液润洗 B、锥形瓶未用待测液润洗
C、滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D、滴定时将标准液溅出锥形瓶外
查看答案和解析>>
科目:高中化学 来源: 题型:
将总物质的量为n mol的钠和铝的混合物(其中钠的物质的量分数为x),投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V L 。下列关系式中正确的是 ( )
。下列关系式中正确的是 ( )
A.x=V/(11.2n) B.0<x≤0.5
C.V=33.6n(1-x) D.11.2n<V≤22.4n
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,一个装满氯气的容器的质量为74.6 g,若装满氮气时总质量为66 g,则此容器的容积是 ( )
A.22.4 L B.44.8 L
C.11.2 L D.4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业、硫酸工业的生产工艺 流程如图所示 。
。
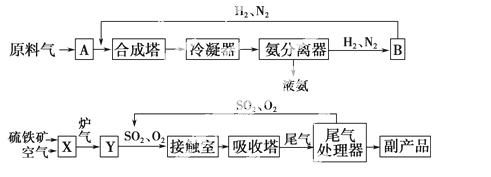
合成塔和接触室中的反应分别为
N2(g)+3H2(g) 2NH3(g) ΔH<0;
2SO2(g)+O2(g) 2SO3(g) ΔH<0。
(1)写出流程中设备的名称:B________,X________。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是___________________。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是________(填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是_______________。
(5)工业生产中常用氨-酸法进行尾气脱硫,以达到消 除污染、
除污染、 废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
(6)根据化学 平衡移动原理,下列条件或措施合理的是________(填序号)。
平衡移动原理,下列条件或措施合理的是________(填序号)。
①合成氨工业在高压下进行
②合成氨工业和硫酸工业都使用催化剂
③及时将氨液化而分离
④硫酸工业中,净化后的炉气中要有过量空气
⑤合成氨工业和硫酸工业都采用适宜的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com