
| A、蒸发结晶时,应将溶液蒸干后才停止加热 |
| B、蒸馏中,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
| D、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释至刻度线 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4项 | B、5项 | C、6项 | D、7项 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验器材 | 相应实验 |
| A | 坩埚、玻璃棒、酒精灯、泥三角 | 从食盐水中获得NaCl晶体 |
| B | 漏斗、滤纸、烧杯、玻璃棒 | 除去氢氧化铝胶体中的泥沙 |
| C | 分液漏斗、烧杯 | 利用四氯化碳萃取溴水中的溴 |
| D | 圆底烧瓶、分液漏斗、酒精灯、洗气瓶、集气瓶、导管、石棉网 | 用MnO2和浓盐酸制取干燥、纯净的氯气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有SO42- |
| B、向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- |
| C、取少量久置的Na2SO3样品于试管中加水溶解,再加盐酸酸化,然后加BaCl2溶液,若加HCl时有气体产生,加BaCl2时有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
| D、能使湿润的碘化钾淀粉试纸变蓝的一定是Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
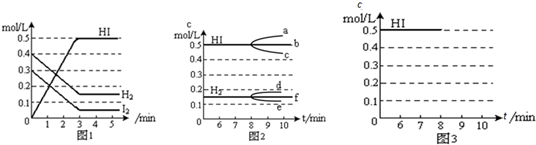
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①和④ | B、②和③ |
| C、②③④ | D、只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯的结构简式可以表示为CH2CH2 |
| B、收集乙烯可用排空气法 |
| C、可作香蕉等水果的催熟剂 |
| D、燃烧时火焰明亮,同时产生黑烟 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com