
����Ŀ����ˮ��Դ�ḻ����ˮ����Ҫ����Na+��K+��Mg2+��Cl����SO42����Br����CO32��HCO3�������ӣ��������ú�ˮ��Դ�ͱ����������ҹ��ɳ�����չ����Ҫ��֤��
��1����������ȼ��ú�ŷŵ�SO2�����һϵ�л�������̬���⣮���ú�ˮ������һ����Ч�ķ������乤��������ͼ��ʾ�� 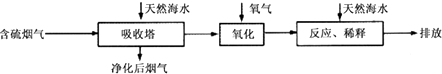
��i����Ȼ��ˮ��pH��8���������ԣ������ӷ���ʽ������Ҫԭ�� ��
��ii����Ȼ��ˮ�����˺���������Ҫ��O2���������������䷴Ӧ�Ļ�ѧ����ʽ����������ġ���ˮ����Ҫ�ô�������Ȼ��ˮ��֮�������ŷţ��ò�������ҪĿ�����к͡�ϡ�;�����������ˮ�����ɵ��ᣮ
��iii�������е�SO2����ijŨ��NaOH��Һ���յõ�Na2SO3��NaHSO3�����Һ����������Һ�����ԣ�����Һ��c��Na+��=���ú�����Ũ�ȵĴ���ʽ��ʾ����
��iv����ͬ���ʵ�����SO2��NH3����ˮ������Ӧ�����ӷ���ʽΪ �� ������Һ��c��H+����c��OH����=������ĸ��ţ���
A��c��SO32������c��H2SO3�� B��c��SO32����+c��NH3 �� H2O����c��H2SO3��
C��c��HSO3����+c��SO32������c��NH4+�� D��c��HSO3����+2c��SO32������c��NH4+��
��2���ؽ������ӶԺ������������������Ⱦ��ij��������ˮ��pH=2.0���ѡ�1g/mL���к���Ag+��Pb2+���ؽ������ӣ���Ũ�ȸ�ԼΪ0.1mol/L���ŷ�ǰ���ó�������ȥ���������ӣ������й��������£�
���� | AgI | AgOH | Ag2S | pbI2 | Pb��OH��2 | PbS |
Ksp | 8.3��10��17 | 5.6��10��8 | 6.3��10��50 | 7.1��10��9 | 1.2��10��15 | 3.4��10��28 |
��i������Ϊ����ˮ��Ͷ��������ĸ��ţ�������Ч����ã�
A��NaOH B��Na2S C��KI D��Ca��OH��2
��ii���������ʯ�Ҵ���������ˮ��ʹ��Һ��pH=8.0��������ķ�ˮ��c��Pb2+��= ��
��iii�������ʳ�δ���ֻ��Ag+�ķ�ˮ����ô�����ķ�ˮ��NaCl����������Ϊ0.117%���ѡ�1gmL��1����������Ҫ���ŷű�Ϊc��Ag+������1.0��10��8mol/L���ʸù���������ķ�ˮ��c��Ag+��= �� ����֪KSP��AgCl��=1.8��10��10��
���𰸡�
��1��CO32��+H2O?HCO3��+OH����HCO3��+H2O?H2CO3+OH����2H2SO3+O2�T2H2SO4��2c��SO32����+c��HSO3������SO2+NH3?H2O=NH4++HSO3����BD
��2��B��1.2��10��3mol?L��1��9��10��9 mol?L��1
���������⣺��1����i����ˮ����Ҫ����Na+��K+��Mg2+��Cl����SO42����Br����CO32����HCO��3�����ӣ�����Щ�������ܷ���ˮ�����CO32����HCO��3���ӣ�CO32��+H2OHCO3��+OH�� �� HCO3��+H2OH2CO3+OH������ˮ��ʼ��ԣ�������Ȼ��ˮ��pH��8���������ԣ�
���Դ��ǣ�CO32��+H2OHCO3��+OH����HCO3��+H2OH2CO3+OH������ii����Ȼ��ˮ�����˺���������Ҫ��O2��������������������H2SO3����Ϊ���ᣬ�÷�ӦΪ2H2SO3+O2=2H2SO4 �� ������ġ���ˮ����Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ������к�ϡ�;�����������ˮ�����ɵ��ᣨH+����
���Դ��ǣ�2H2SO3+O2�T2H2SO4����iii�������е�SO2����ijŨ��NaOH��Һ���յõ�Na2SO3��NaHSO3�����Һ����������Һ�����ԣ���Һ�д��ڵ���غ�c��Na+��+c��H+��=2c��SO32����+c��HSO3����+c��OH������c��H+��=c��OH�������õ�c��Na+��=2c��SO32����+c��HSO3������
���Դ��ǣ�2c��SO32����+c��HSO3��������iv����ͬ���ʵ�����SO2��NH3����ˮ������Ӧ����̼����泥���Ӧ�����ӷ���ʽΪSO2+NH3+H2O�TNH4++HSO3�� �� ��Һ�д��ڵ���غ㣺c��HSO3����+2c��SO32����+c��OH����=c��H+��+c��NH4+����c��H+����c��OH����=c��HSO3����+2c��SO32������c��NH4+����D��ȷ��C������Һ�д��������غ㣺c��NH4+��+c��NH3H2O��=c��HSO3����+c��SO32����+c��H2SO3������ϵ���غ�������غ��֪c��H+����c��OH����=c��HSO3����+2c��SO32������c��NH4+��=c��SO32����+c��NH3 �� H2O����c��H2SO3��������A����B��ȷ�����Դ��ǣ�SO2+NH3+H2O�TNH4++HSO3����BD����2����i���ɱ����е����ݿ�֪���ܶȻ�ԽС��Խ��ת��Ϊ��������Ȼֻ��������ܶȻ�С����Ӧѡ�����ƣ�
���Դ��ǣ�B����ii����Pb��OH��2���ܶȻ�Ϊ1.2��10��15 �� pH=8.0��c��OH����=10��6molL��1 �� ��c��Pb2+��= ![]() =1.2��10��3molL��1 ��
=1.2��10��3molL��1 ��
���Դ��ǣ�1.2��10��3molL��1����iii����ˮ��NaCl����������Ϊ0.117%���ѡ�1gmL��1����c��Cl����=c��NaCl��= ![]() =0.02mol/L��
=0.02mol/L��
Ksp��AgCl��=c��Ag+��c��Cl����=1.8��10��10mol2L��2 �� ��c��Ag+��= ![]() =9��10��9molL��1 �� ����Ҫ���ŷű�Ϊc��Ag+������1.0��10��8molL��1 �� ��Ȼ9��10��9molL��1��1.0��l0��8molL��1 ��
=9��10��9molL��1 �� ����Ҫ���ŷű�Ϊc��Ag+������1.0��10��8molL��1 �� ��Ȼ9��10��9molL��1��1.0��l0��8molL��1 ��
���Դ��ǣ�9��10��9molL��1 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��нϴ�����Cl����CO ![]() ��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ� �� �ٵμ�AgNO3��Һ���ڹ��ˣ��۵μ�Mg��NO3��2��Һ���ܵμ�Ba��NO3��2��Һ��
��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ� �� �ٵμ�AgNO3��Һ���ڹ��ˣ��۵μ�Mg��NO3��2��Һ���ܵμ�Ba��NO3��2��Һ��
A.�٢ڢۢڢ�
B.�ܢڢ٢ڢ�
C.�٢ڢܢڢ�
D.�ܢڢۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������к��������Ҵ����ʣ����з����п��Գ�ȥ�����ʵ���(�� ��)
A. ����Ũ���Ტ���ȵ�170����ʹ�Ҵ������ϩ���ݳ�
B. ���������Ტ���ȣ�ʹ�Ҵ�ת��Ϊ������
C. ��������ƣ�ʹ�Ҵ�������Ӧ����ȥ
D. ��ˮ�����÷ֲ���÷�Һ©������ȥˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ã��缫��Ϊ���Ե缫��������SO2 �� ���������ų�����Һ����NO2 �� ����˵����ȷ���ǣ� �� 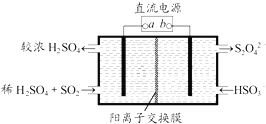
A.aΪֱ����Դ�ĸ���
B.�����ĵ缫��ӦʽΪ��2HSO3��+2H++e���TS2O42��+2H2O
C.�����ĵ缫��ӦʽΪ��SO2+2H2O��2e���TSO42��+4H+
D.���ʱ��H+��������ͨ�������ӽ���Ĥ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��������������Һ�У��ܹ�����������ǣ�������
A.NH4+��Cl����Fe2+��K+B.Na+��CO32����K+��Cl��
C.Cl����Ba2+��Na+��SO42��D.K+��SO42����OH����Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ�ļס��ҡ������־��壺

�����
(1)����Ļ�ѧʽ(XΪ������)Ϊ________��
(2)�Ҿ�����A��B��C�������ӵĸ�������________��
(3)��������ÿ��D��Χ���E�ĸ�����________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ��,��ԭ��������������,����Aԭ�Ӻ���������δ�ɶԵ���;A��B���γ����ӻ�����B3A2;CԪ���ǵؿ��к�����ߵĽ���Ԫ��;Dԭ�Ӻ����M���������ԳɶԵ���;Eԭ�Ӻ��������ֻ��1������,���������Ӿ������������������Ϣ,�ش���������(����ʱ,A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ):
(1)��E�����������5��Ԫ�ص�ԭ�Ӻ�������Ų�ʽ�� ,A��B��C��D�ĵ�һ��������С�����˳��Ϊ ��
(2)B���Ȼ�����۵�Զ����C���Ȼ�����۵�,������ ��
(3)A���⻯������ (����ԡ��Ǽ��ԡ�)����,D�ĵͼ���������ӵ����幹���� ��
(4)A��E�γɵ�ij�ֻ�����ľ����ṹ��ͼ��ʾ,���仯ѧʽΪ (ÿ�������ʾ1��ԭ��)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ѱ�ҵ�ĸ���ƷFeSO4[��Al2��SO4��3�������ؽ�������]������������ؼ��ߴ���ϸ�����������乤��������ͼ1�� 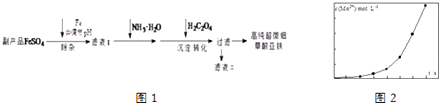
��֪����5Fe2++MnO ![]() +8H+�T5Fe3++Mn2++4H2O
+8H+�T5Fe3++Mn2++4H2O
��5C2O42��+2MnO ![]() +16H+�T10CO2��+2Mn2++8H2O
+16H+�T10CO2��+2Mn2++8H2O
��1���������̵ķ�Ӧ�¶�Ϊ40�棬�¶Ȳ��˹��ߵ�ԭ����˿��Ƴ����������⣬���� ��
��2����Һ�����ɵõ�����Ʒ ��
��3��ʵ���Ҳⶨ�ߴ���ϸ����������ɵIJ�������Ϊ��
����1��ȷ����һ��������������Ʒ������25mL 2molL��1��H2SO4�ܽ⣮
����2����0.2000molL��1��KMnO4��Һ�ζ������������30.40mL��
����3����ζ������Һ�м���2g Zn�ۺ�5mL 2molL��1��H2SO4��Һ����Fe3+��ԭΪFe2+ ��
����4�����ˣ���Һ��������KMnO4��Һ�ζ���������Һ10.40mL��
����Ʒ��C2O42�������ʵ���Ϊ ��
��4����һ�������������Һ���ữ�IJ���������Һ��ϣ���÷�ӦҺ��Mn2+��Ũ���淴Ӧʱ��t�ı仯��ͼ2���������ֱ仯���Ƶ�ԭ�����Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ����һ���¹ʵ�Ԥ���ʹ���������ȷ����
A. ȼ�ŵľƾ��ƴ�ʧ��Ӧ������ˮ����
B. Ƥ����մ������Ũ���ᣬ��������NaOH��ϴ��
C. ��������ε�ʵ��̨�ϣ�������ʪĨ������������ˮ��ϴĨ��
D. ����ʳ����Һʱ������Һ�ηɽ�����Ӧ������ˮ��ȴ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com