
【题目】在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8、PtNi20等。
(1)某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于___(填“晶体”或“非晶体”)。区分晶体和非晶体最可靠的方法是对固体进行___实验。
(2)实验证明,PtCl2(NH3)2的结构有两种:A呈棕黄色,有抗癌活性,在水中的溶解度为0.258g;B呈淡黄色,无抗癌活性,在水中的溶解度为0.037g。试推测PtCl2(NH3)2的空间构型是__(填“四面体形”或“平面四边形”);请画出A的结构图示___。
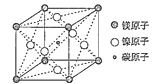
(3)据报道只含镁、镍和碳三种元素的晶体具有超导性,该晶体的晶胞结构如图所示,写出该晶体的化学式__。晶体中每个镁原子周围距离最近的镍原子有__个。
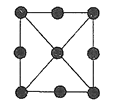
(4)金属铂立方晶体的二维投影图如图所示。若金属铂的密度为dgcm-3,设阿伏加德罗常数的值为NA,则晶胞参数a=__pm(列出计算式即可)。
【答案】晶体 X-射线衍射 略 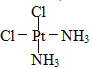 MgCNi3 12
MgCNi3 12 ![]() ×1010
×1010
【解析】
(1)晶体具有自范性,可通过X-射线衍射实验进行鉴别;
(2)根据Pt(NH3)2Cl2可以形成两种固体知:Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上;根据水的极性及相似相溶原理分析可知,A的分子极性较大,据此画出结构图;
(3)根据均摊法计算晶胞中各原子个数,进而确定化学式;Mg原子处于顶点,与之最近的Ni原子处于面心,每个顶点为12面共用;
(4)根据金属Pt的晶胞的二维投影,晶胞为立方晶胞,为面心立方最密堆积,根据密度公式d=![]() 计算晶胞参数a。
计算晶胞参数a。
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于晶体,可通过X-射线衍射方法鉴别;
(2)Pt(NH3)2Cl2可以形成两种固体,说明Pt(NH3)2Cl2分子是平面四边形结构,若为四面体结构则只有一种固体形式,不存在同分异构体,共有两种同分异构体,其中A在水中的溶解度大于B,则A为极性分子,结构图为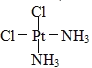 ;
;
(3)碳原子位于晶胞体心,只有1个C原子,镁位于顶点,晶胞中Mg原子数目为8×![]() =1,镍位于面心,每个镍原子被两个晶胞共用,故每个晶胞中镍原子个数为6×
=1,镍位于面心,每个镍原子被两个晶胞共用,故每个晶胞中镍原子个数为6×![]() =3,故晶体化学式为MgCNi3;Mg原子处于顶点,与之最近的Ni原子处于面心,每个顶点为12面共用,所以晶体中每个镁原子周围距离最近的镍原子有12个;
=3,故晶体化学式为MgCNi3;Mg原子处于顶点,与之最近的Ni原子处于面心,每个顶点为12面共用,所以晶体中每个镁原子周围距离最近的镍原子有12个;
(4)根据金属Pt的晶胞的二维投影,晶胞为立方晶胞,为面心立方最密堆积,一个晶胞中含有Pt的个数为8×![]() +6×
+6×![]() =4,晶胞的物质的量为
=4,晶胞的物质的量为![]() mol,质量为
mol,质量为![]() g,一个晶胞的体积为V=a3cm3,所以晶胞的密度d=
g,一个晶胞的体积为V=a3cm3,所以晶胞的密度d=![]() g/ cm3,a=
g/ cm3,a=![]() cm=
cm=![]() ×1010pm。
×1010pm。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
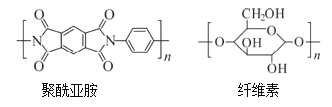
【题目】嫦娥三号探测器携国旗在月面探测时,要经受高低温交替变化、强辐射等恶劣环境的考验。为解决棉布(主要成分是纤维素)和丝绸(主要成分是蛋白质)等材料制作的国旗在此环境下易变色和开裂的问题,科研团队通过大量模拟实验,最终选择了某种合成聚酰亚胺作为制作国旗的基本材料,从而使鲜艳夺目的五星红旗展现在月球上!请回答下列问题:
(l)从组成和结构看,如图所示的聚酰亚胺比纤维素多一种元素,该元素的符号是________;纤维素中所含的官能团除醚键(![]() )外,另一种官能团是_____________。
)外,另一种官能团是_____________。
(2)月球表面温度通常在![]() 之间交替变化。为使制作国旗的材料能适应温度巨变,科研工作者在模拟实验中,先将聚酰亚胺制作的五星红旗置于极度低温的_________(填下表中制冷剂的名称)环境中数秒,取出后马上放进________(填“略高于”或“低于”)130℃的高温恒温箱中数分钟,如此反复实验了数百次。
之间交替变化。为使制作国旗的材料能适应温度巨变,科研工作者在模拟实验中,先将聚酰亚胺制作的五星红旗置于极度低温的_________(填下表中制冷剂的名称)环境中数秒,取出后马上放进________(填“略高于”或“低于”)130℃的高温恒温箱中数分钟,如此反复实验了数百次。
制冷剂 | 干冰 | 干冰-乙醚 | 液氮 |
极限制冷温度/℃ |
|
|
|
(3)聚酰亚胺、纤维素、蛋白质均为高分子化合物,但与聚酰亚胺不同,纤维素和蛋白质都属于____(填“合成”或“天然”)高分子化合物。这三种高分子化合物在酸性条件下均可水解,其中,纤维素水解的最终产物为单糖,该单糖的名称是______(填“葡萄糖”或“果糖”);蛋白质水解的最终产物为______。
(4)随着社会发展,有机固体废弃物的数量剧增,对这类废弃物可用封闭式焚烧或卫生填埋处理。相比卫生填埋,封闭式焚烧的优点是减小废弃物的体积,同时可利用燃烧产生的热量发电,该发电过程实现了“____能→热能→机械能→电能”的转化;但这种处理方法也存在成本高、可能产生有害______(填“气体”或“液体”)污染环境的缺点。废弃塑料袋是生活中常见的有机固体废弃物,填埋、焚烧都有缺点,因此,我们有必要通过________(填一种方法)来减少这类固体废弃物的产生。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A.单位时间内消耗a mol A,同时生成3a mol CB.容器内B的浓度不再变化
C.混合气体的物质的量不再变化D.A的消耗速率等于C的生成速率的![]() 倍
倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有________种能量不同的电子;很多不饱和有机物在Ni催化下可以H2发生加成反应,如①CH2═CH2、②HC≡CH、③ ![]() 、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来有多个关于超高压下新型晶体的形成与结构的研究报道。NaCl晶体在50~300GPa的高压下和Na或Cl2反应,可以形成不同组成、不同结构的晶体。如图给出其中三种晶体的晶胞(大球为氯原子,小球为钠原子),关于这三种晶胞的说法正确的是( )

A.晶胞Ⅰ中钠原子的配位数为12
B.晶胞Ⅱ中含有6个钠原子
C.晶胞Ⅲ所对应晶体的化学式为Na2Cl
D.三种晶体均是由NaCl晶体在50~300GPa的高压下和Na反应所得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,其单质及化合物在航天、军事、航海、医疗等领域都有着重要的应用。请回答下列问题:
(1)在元素周期表中,锆元素与钛元素同族,则锆元素位于__区。
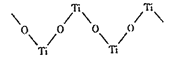
(2)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形成存在的钛酰阳离子,其结构如图所示,若阳离子所带电荷为+n,则该离子中钛原子数为__。
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个Al原子与__个N原子相连,与同一个N原子相连的Al原子构成的立体构型为___,氮化铝晶体属于___晶体。
(4)Ti3+可形成配位数为6的两种配合物晶体(一种是紫色,一种是绿色),组成皆为TiCl36H2O。向含有0.01mol绿色配合物晶体的水溶液中加入过量硝酸银溶液,产生0.02molAgCl沉淀,则绿色配合物晶体的化学式为__。
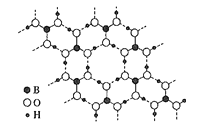
(5)硼与铝同族,硼酸晶体是片层结构,其中一层的结构如图所示,层内的分子以氢键相连。含1mol硼酸的晶体中有__mol氢键。图中所示最外层已达8原子结构的原子是__(填元素符号),H3BO3晶体中B原子个数与极性键个数比为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,把0.5molN2O4通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达平衡,此时容器内压强为开始时的1.6 倍。下列说法正确的是
A.前2s以N2O4的浓度变化表示的平均反应速率为0.01mol·L-1·s-1
B.在2s时体系内的压强为开始时的1.1倍
C.在平衡时体系内N2O4的物质的量为0.25mol
D.平衡时,N2O4的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比鲁卡胺(分子结构见合成线路)是有抗癌活性,其一种合成路线如图:
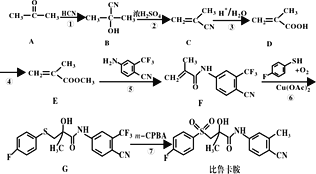
回答下列问题
(1)A的化学名称为__。
(2)D中官能团的名称是__。
(3)反应④所需试剂、条件分别为__、__。
(4)写出⑤的反应方程式__。
(5)F的分子式为__。
(6)写出与E互为同分异构体,且符合下列条件的化合物的结构简式__。
①所含官能团类别与E相同;②核磁共振氢谱为三组峰,峰面积比为1:1:6
(7)参考比鲁卡胺合成的相关信息,完成如图合成线路(其他试剂任选)___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是可逆反应A+2B![]() 2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
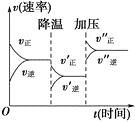
A.该反应的正反应是吸热反应
B.若A,B是气体,则D一定是纯液体或固体
C.该反应的平衡常数始终没变
D.A的转化率最终增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com