
【题目】Al﹣AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是( ) 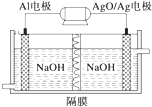
A.当电极上析出0.54 g Ag时,电路中转移的电子为0.01 mol
B.该隔膜是阳离子交换膜
C.Al电极的反应式为:Al﹣3e﹣+3OH﹣=Al(OH)3
D.正极的电极反应式为:AgO+2e﹣+2H+=Ag+H2O
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】下列关于浓硫酸的叙述中正确的是
A. 将水沿着玻璃棒慢慢地注入盛有浓硫酸的量筒中稀释,并不断搅拌
B. 运输时可以将浓硫酸密封装在铁罐中
C. 浓硫酸滴到硫酸铜晶体中的现象体现了浓硫酸的脱水性
D. 少量浓硫酸滴入紫色石蕊溶液中,溶液会褪为无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容的容器中进行反应:2HIH2+I2(正反应为吸热反应),反应物的浓度由0.1mol/L降到0.06mol/L需要20s,那么由0.06mol/L降到0.036mol/L所需时间为( )
A.等于10 s
B.等于12 s
C.大于12 s
D.小于12 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池示意图如图所示,有关说法正确的是( ) 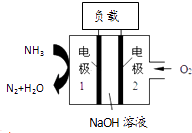
A.电极2发生氧化反应
B.电池工作时,Na+向负极移动
C.电流由电极1经外电路流向电极2
D.电极1发生的电极反应为:2NH3+6OH﹣﹣6e﹣=N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的工业制法合理的是
A. 玻璃是纯碱和石灰石高温反应制得
B. 高炉炼铁中通过焦炭直接还原赤铁矿
C. 工业上通过电解NaCl溶液获取Na单质
D. 高纯硅的制备是通过氢气还原四氯化硅实现的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的转化在实际工业生产、生活中具有重要的意义。
(1)已知工业上合成氨N2(g)+3H2(g)![]() 2NH3(g)的能量变化如图所示,在一定温度下,向2 L的恒容密闭容器中投入2.2 mol N2和2.6 mol H2,经10 min达到平衡,测得以氢气表示的平均速率为0.03mol·L-1·min-1
2NH3(g)的能量变化如图所示,在一定温度下,向2 L的恒容密闭容器中投入2.2 mol N2和2.6 mol H2,经10 min达到平衡,测得以氢气表示的平均速率为0.03mol·L-1·min-1
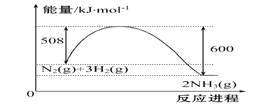
①该反应的热效应△H=______________
②反应达到平衡后放出的热量为__________kJ,此时N2的转化率为___________;在该温度下,反应的平衡常数K=__________
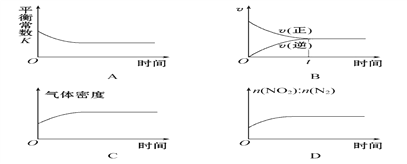
(2)利用炽热的活性炭可以处理NO2,反应原理为2C(s)+2NO2(g)![]() 2CO2(g)+N2(g),一定温度下,将一定量的活性炭和NO2加入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填序号)。
2CO2(g)+N2(g),一定温度下,将一定量的活性炭和NO2加入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者大于后者的是( ) ①C(s)+O2(g)═CO2(g);△H1 C(s)+ ![]() O2(g)═CO(g);△H2
O2(g)═CO(g);△H2
②S(s)+O2(g)═SO2(g);△H3 S(g)+O2(g)═SO2(g);△H4
③H2(g)+ ![]() O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8 .
A.①
B.④
C.②③④
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.保持体积不变,增加H2O(g)的物质的量
B.将容器的体积缩小一半
C.保持体积不变,充入Ar使压强增大
D.保持压强不变,充入Ar使体积增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com