
[ ]
科目:高中化学 来源: 题型:阅读理解
| 信息卡 常温下碳酸钙难溶于水,氢氧化钙微溶于水,氯化钙易溶于水.次氯酸钙易溶于水,酸性条件下不稳定、100°C时发生分解反应. 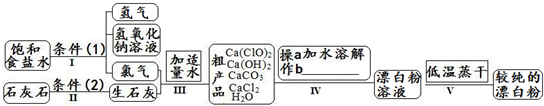 (1)流程I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是 2 2 mol?L-1.(2)写出流程I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目:   高温 高温 .(3)流程III中发生两个反应,写出其中的氧化还原反应的化学反应方程 2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O 2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O .其中氧化剂是Cl2 Cl2 ;还原剂是Cl2 Cl2 .(写化学式)(4)流程IV中操作b是: 过滤 过滤 .(写名称)(5)流程V进行低温蒸干的原因是: Ca(ClO)2在100°C时发生分解反应 Ca(ClO)2在100°C时发生分解反应 .(6)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因 Ca(ClO)2+CO2+H2O═CaCO3+2HClO Ca(ClO)2+CO2+H2O═CaCO3+2HClO .(7)氯水和次氯酸钙都能起漂白、消毒作用.是因为它们都能产生同一种物质,写出氯气与水反应产生该物质的化学方程式 Cl2+H2O  HCl+HClO HCl+HClOCl2+H2O . HCl+HClO HCl+HClO(8)在酸性条件下次氯酸钙的氧化性比氯气强,能将溴离子氧化成溴单质,而次氯酸钙中的氯元素则被还原为负一价的氯离子,氧元素则转化为水.试写出次氯酸钙和稀盐酸的混合物与溴化钠反应的化学方程式: Ca(ClO)2+4HCl+4NaBr=CaCl2+4NaCl+2Br2+2H2O Ca(ClO)2+4HCl+4NaBr=CaCl2+4NaCl+2Br2+2H2O .
查看答案和解析>> 科目:高中化学 来源: 题型: 漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙.如图为制取漂白粉的工业流程简图. 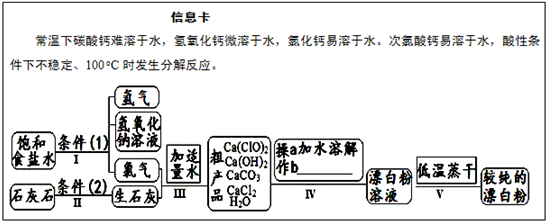 (1)流程 I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是 2 2 mol?L-1.(2)写出流程 I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目:   高温 高温 .(3)流程 III中发生两个反应,写出其中一个的氧化还原反应的化学反应方程 2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O 2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O .(4)流程 IV中操作b是: 过滤 过滤 .(写名称)(5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因 Ca(ClO)2+CO2+H2O═CaCO3+2HClO Ca(ClO)2+CO2+H2O═CaCO3+2HClO .查看答案和解析>> 科目:高中化学 来源:河北省承德市宽城一中2009-2010学年高一第一学期期中考试化学试题 题型:058 下图中A、B、C是常见的化学实验装置,请回答下列问题: 
(1)实验里用A装置加热可制取氯气,为得到纯净干燥的氯气,可让A中逸出的气体在进入收集装置前依次通过分别装有________和________的两个洗气瓶B,此时应从B装置中的________(填a或b)口通入气体. (2)铜在氯气中剧烈燃烧,使集气瓶充满________色的________(填烟或雾),有关化学方程式为________; (3)为防止氯气尾气污染空气,可用________溶液吸收多余的氯气,原理是(用离子方程式表示)________. 根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,工业上生产漂白粉的化学方程________.漂白粉的主要成分是________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体主要是________(用字母代号填). A.O2 B.Cl2 C.CO2 D.HClO 查看答案和解析>> 科目:高中化学 来源:2011-2012学年江苏省常州市金坛市高一(上)期中化学试卷(解析版) 题型:解答题 漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙.下图为制取漂白粉的工业流程简图.
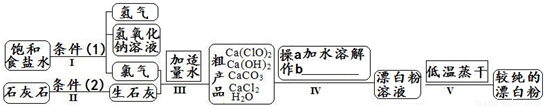 (1)流程I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是______ mol?L-1. (2)写出流程I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目:______.流程II的反应条件(2)是______. (3)流程III中发生两个反应,写出其中的氧化还原反应的化学反应方程______.其中氧化剂是______;还原剂是______.(写化学式) (4)流程IV中操作b是:______.(写名称) (5)流程V进行低温蒸干的原因是:______. (6)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因______. (7)氯水和次氯酸钙都能起漂白、消毒作用.是因为它们都能产生同一种物质,写出氯气与水反应产生该物质的化学方程式______. (8)在酸性条件下次氯酸钙的氧化性比氯气强,能将溴离子氧化成溴单质,而次氯酸钙中的氯元素则被还原为负一价的氯离子,氧元素则转化为水.试写出次氯酸钙和稀盐酸的混合物与溴化钠反应的化学方程式:______. 查看答案和解析>> 科目:高中化学 来源:2012-2013学年浙江省绍兴市诸暨市湄池中学高一(上)期中化学试卷(平行班)(解析版) 题型:填空题 漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙.如图为制取漂白粉的工业流程简图.  (1)流程 I 得到浓度为80g?L-1氢氧化钠溶液,其物质的量浓度是 mol?L-1. (2)写出流程 I发生反应的化学反应方程式,并用双线桥表示其电子转移的方向和数目: .流程 II的反应条件(2)是 . (3)流程 III中发生两个反应,写出其中一个的氧化还原反应的化学反应方程 . (4)流程 IV中操作b是: .(写名称) (5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因 . 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |