
| A. | NH4Cl H2O CO2 | B. | NaCl MgCl2 Na2O | ||
| C. | H2O Na2O CO2 | D. | CaCl2 NaOH H2SO4 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,铵盐中存在离子键,据此分析解答.
解答 解:A.NH4Cl中存在离子键和共价键,H2O、CO2中只存在共价键,所以化学键类型不同,故A错误;
B.NaCl、MgCl2、Na2O中金属元素和非金属元素之间只存在离子键,所以化学键类型相同,故B正确;
C.Na2O中只存在离子键,CO2、H2O中只存在共价键,所以化学键类型不同,故C错误;
D.CaCl2中只存在离子键,NaOH中存在离子键和共价键,H2SO4中只存在共价键,所以化学键类型不同,故D错误;
故选B.
点评 本题考查了化学键的判断,题目难度不大,明确物质的构成微粒及微粒间的作用力是解本题关键,注意:氯化钙中两个氯离子之间不存在化学键、氯化铵是全部由非金属元素组成的离子化合物,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 砹(At)是第VIIA族元素,其氢化物的穆定性大于HCl | |
| B. | 铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应 | |
| C. | 第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 | |
| D. | 第3周期金属元素最高价氧化物对应的水化物,其碱性随原子序数的增大而减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向蒸馏水中滴加浓硫酸的过程中,Kw保持不变 | |
| B. | 酸与碱溶液恰好完全反应时所得溶液一定呈中性 | |
| C. | 向醋酸钠溶液中加入少量冰醋酸,水的电离度减小 | |
| D. | 广泛pH试纸能够测出溶液的精确pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 将过量氨水加入AlCl3溶液中:Al3++4OH-═AlO2-+2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+═3I2+3H2O | |
| D. | 向NaHCO3溶液中加入等物质的量的Ca(OH)2:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
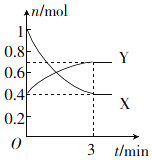 一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2 (g)(红棕色)?N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示.
一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2 (g)(红棕色)?N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | O=O | H-O |
| 键能(KJ/mol) | 436 | 496 | 463 |
| A. | 242KJ | B. | 442 KJ | C. | 484 KJ | D. | 448KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
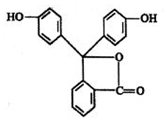 酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图:
酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8mol | B. | 1.2mol | C. | 0.9mol | D. | 0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com