
【题目】下列物质的溶液中所含离子种类最多的是( )
A. Na2SB. Na3PO4C. NaHCO3D. H2SO4
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
①热稳定性:H2O> HF> H2S ②最外层两个电子的元素 , 不一定在第IIA族
③IIA族元素的阳离子与上一周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中, 在离核较近的区域内运动的电子能量较高
⑥氯的各种含氧酸的酸性由弱到强排列为 HClO<HClO2<HClO3<HClO4
⑦两个非金属元素原子间只可能形成共价键, 而含金属元素的化合物中一定含离子键
A. ②④⑥ B. ①⑤⑥ C. ②③④ D. ①⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宋代著名法医学家宋慈的《洗冤集录》中有一银针验毒的记载,“银针验毒”的原理是4Ag + 2H2S + O2 =" 2X" + 2H2O,下列说法正确的是
A. X的化学式为AgS B. 银针验毒时,空气中氧气失去电子
C. 反应中Ag和H2S均是还原剂 D. 每生成1mo1X,反应转移2mo1e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中,正确的是:
A. 以海水为原料制得精盐,再电解精盐的水溶液制取钠
B. 用海水、石灰乳等为原料,经一系列过程制得氧化镁,用H2还原氧化镁制得镁
C. 以铁矿石、焦炭、空气、石灰石等为原料,通过反应产生的CO在高温下还原铁矿石制得铁
D. 从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5:有机化学基础】
维拉佐酮是临床上使用广泛的抗抑郁药,其关键中间体G的合成路线如下:
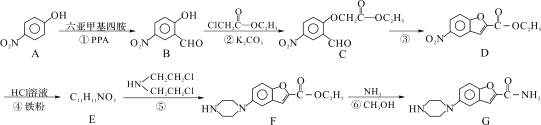
已知:![]()
请回答下列问题:
(1)C中含氧官能团的名称_________。(任写两种)
(2)反应④的反应类型是:_________,G的分子式为:_________。
(3)下列有关说法错误的是_________。
a.B遇FeCl3溶液显紫色且能发生银镜反应
b.A、B两种物质不可用核磁共振氢谱或红外光谱区别
c.C能发生取代、加成、氧化、还原反应
d.1 mol D能与2 mol NaOH反应
(4)反应②的化学方程式:_________;反应②加入K2CO3的作用是_________。
(5)写出同时满足下列条件B的一种同分异构体的结构简式:_________。
①能发生银镜反应
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应
③核磁共振氢谱有三组峰
(6)已知:![]()
请以甲苯、乙醇等为原料制备 ![]() ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见题干)______
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见题干)______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸钠可以用于制备火箭推进剂高氯酸铵。以粗盐为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如下:

(1)“精制”中,由粗盐(含Ca2+、Mg2+、SO42-等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用
(2)“电解”分2步进行,其反应分别为NaCl+3H2O![]() NaClO3+3H2↑ NaClO3+H2O
NaClO3+3H2↑ NaClO3+H2O![]() NaClO4+H2↑
NaClO4+H2↑
(3)“除杂”的目的是除去少量未被电解的NaClO3,该反应的化学方程式为: ,
(4)“分离”的操作分别是加热浓缩、 、冷却结晶、过滤、洗涤、干燥。(各物质的溶解度如右图所示)
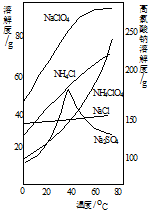
(5)室温下将得到的高氯酸钠晶体加入氯化铵饱和溶液中,反应的离子方程式为:
(6)为确定所得高氯酸钠晶体的纯度(含有少量Na2SO4杂质),进行如下实验:
①准确称取3.00 g样品加水充分溶解,所得溶液转移至容量瓶并配置成100 mL溶液。
②量取25.00 mL溶液,加入足量的KI溶液充分反应(ClO4-被还原成Cl-),再滴加1.000 mol·L-1 Na2S2O3溶液进行反应(反应为I2+2 Na2S2O3=2 NaI+ Na2S4O6),恰好消耗40.00 mL Na2S2O3溶液。
根据以上数据计算样品中高氯酸钠晶体纯度为: (写出计算过程,保留四位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
![]()
①铜元素位于周期表_________区;Cu+的基态价电子排布图_________;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为_________(元素符号表示)。
②SO42-中心原子的杂化方式为_________,SO32-的价层电子互斥模型为_________。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式_________。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是_________。
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_________。
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为_________,用含有a、ρ的代数式表示的阿伏加德罗常数为:_________ mol-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为达到下列实验目的,所采用的方法合理的是( )
A.溴水中提取溴:分液
B.分离水和汽油的混合物:蒸馏
C.分离饱和食盐水和沙子的混合物:过滤
D.从硝酸钾和氯化钠混合液中获取硝酸钾:萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 冰水混合物 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 氯化铜 | 二氧化硫 |
C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
D | 胆矾 | 食盐水 | 氧化铝 | 碳酸钠 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com