
分析 (1)单质锌在金属活动顺序表中排在银的前面,锌能与银离子之间发生氧化还原反应;
(2)实验室用稀盐酸 与碳酸钙反应制备二氧化碳气体;
(3)二氧化碳过量,氢氧化钙与二氧化碳反应生成碳酸氢钙.
解答 解:(1)单质锌与银离子之间发生氧化还原反应,离子方程式为:Zn+2Ag+=Zn2++2Ag,
故答案为:Zn+2Ag+=Zn2++2Ag;
(2)实验室中用碳酸钙与稀盐酸反应制取二氧化碳,反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(3)氢氧化钙溶液与过量的二氧化碳反应生成碳酸氢钙,反应的离子方程式为:OH-+CO2=HCO3-,
故答案为:OH-+CO2=HCO3-.
点评 本题考查离子方程式的书写,把握发生的反应及离子反应的书写方法为解答的关键,注意离子反应中保留化学式的物质,题目难度不大.


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ③④⑤⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH3Cl和CCl4常温下都是液体 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Fe2+、SO42-、ClO- | B. | NH4+、Mg2+、SO42-、NO3- | ||
| C. | K+、Al3+、S2-、Cl- | D. | Na+、Fe3+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
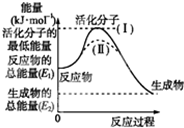 请认真观察图,然后回答问题:
请认真观察图,然后回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com