(2013?昆明一模)【化学一物质结构与性质】
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.
(1)写出Ti基态原子的电子排布
1s22s22p63s23p63d24s2
1s22s22p63s23p63d24s2
.
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物.则电负性C
>
>
B(选填“>”“<”),第一电离能N>O,原因是
N原子中2p轨道处于半充满比较温度,所以第一电离能N>O
N原子中2p轨道处于半充满比较温度,所以第一电离能N>O
.
(3)月球岩石?玄武岩的主要成分为钛酸亚铁(FeTiO
3).FeTiO
3与80%的硫酸反应可生成TiOSO
4.SO
2-4的空间构型为
正四面体
正四面体
,其中硫原子采用
sp3
sp3
杂化,氧原子的价电子排布图为
,任意写出一种SO
2-4的等电子体
ClO4- S2O32- PO43-
ClO4- S2O32- PO43-
.
(4)将TiOSO
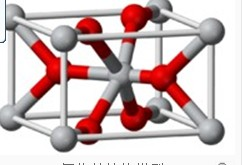
4的稀溶液加热水解后,经进一步反应,可得到钛的某种氧化物.该氧化物的晶胞结构图如图所示.则该氧化物的化学式
TiO2
TiO2
(图中钛原子用“O”表示.氧原子用“O”表示)




 ,SO42-的等电子体有:ClO4- S2O32- PO43-,
,SO42-的等电子体有:ClO4- S2O32- PO43-, ;ClO4- S2O32- PO43-;
;ClO4- S2O32- PO43-;

 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案