
下列热化学方程式正确的是 ( )
A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 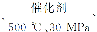 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C.已知在101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为
H2(g)+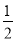 O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为
H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
C
【解析】
试题分析:A.甲烷的燃烧热为890.3 kJ/mol,表示1mol的甲烷完全燃烧产生稳定的氧化物时所放出的热量,在通常情况下,水的稳定状态是液体,不是气态,甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g) ==CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol,错误;B.氮气与氢气合成氨的反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,发生反应的氮气的物质的量小于0.5 mol,因此热化学方程式为N2(g)+3H2(g) 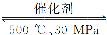 2NH3(g) ΔH<-38.6 kJ/mol,错误;C.1 g H2的物质的量是0.5 mol,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+
2NH3(g) ΔH<-38.6 kJ/mol,错误;C.1 g H2的物质的量是0.5 mol,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+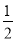 O2(g)==H2O(g) ΔH=-242 kJ/mol,正确;D.中和热为57.3 kJ/mol表示酸碱发生中和反应产生1mol的水所放出的热量,物质发生反应越多,反应放出的热量就越多,所以硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为1/2H2SO4(aq)+KOH(aq)=== 1/2K2SO4(aq)+H2O(l) ΔH=-57.3kJ/mol,错误。
O2(g)==H2O(g) ΔH=-242 kJ/mol,正确;D.中和热为57.3 kJ/mol表示酸碱发生中和反应产生1mol的水所放出的热量,物质发生反应越多,反应放出的热量就越多,所以硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为1/2H2SO4(aq)+KOH(aq)=== 1/2K2SO4(aq)+H2O(l) ΔH=-57.3kJ/mol,错误。
考点:考查热化学方程式书写的正误判断的知识。


科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)2.2.3离子反应 题型:选择题
BaCO3与稀硝酸反应,正确的离子方程式是 ( )
A.Ba2++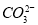 +2H++2N
+2H++2N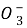 ====Ba(NO3)2+H2O+CO2↑
====Ba(NO3)2+H2O+CO2↑
B.BaCO3+2H++2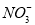 ===Ba(NO3)2+H2O+CO2↑
===Ba(NO3)2+H2O+CO2↑
C.BaCO3+2H+====Ba2++H2O+CO2↑
D.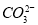 +2H+====H2O+CO2↑
+2H+====H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)1.1.3物质的状态 题型:填空题
(1)0.25 mol某固体A的质量是15 g,A的相对分子质量为 。
(2)在同温、同压、同体积的条件下,H2与气体A的质量之比是1∶8,A的摩尔质量为 。
(3)在25℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,A的摩尔质量为 。
(4)两个同容积的密封容器A、B,在25℃下,A中充入ag A气体,B中充入ag CH4气体,A与B内的压强之比是4∶11,A的摩尔质量为 。
(5)在同温、同压下,相同体积的CH4与气体A的密度之比为1∶4,A的摩尔质量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:实验题
(12分)某研究小组为了探究“铁与水蒸气”的反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒高温下不与水和铁反应).

(1)如何检查该装置的气密性:
(2)写出铁与水蒸气反应的化学方程式
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水。
| 实验步骤 | 预期现象与结论 |
步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的 ,振荡溶解,过滤后将滤液配成250mL溶液,待用。 |
|
步骤2 | 取少量步骤1中滤液于试管中,
|
|
步骤3 | 取少量步骤1中滤液于试管中, |
|
步骤1中加入足量1mol/L CuSO4溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:选择题
下列各组离子在溶液中一定能大量共存的是( )
A.pH=0的溶液中:ClO-、Cu2+、SO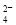 、K+
、K+
B.使pH试纸变红色的溶液中:Fe2+、I-、NO3-、Cl-
C.能够和金属镁反应放出气体的溶液中:Na+、H+、SO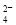 、Cl-
、Cl-
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HS-、Ca2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:选择题
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S ⑤Cl原子最外层有7个电子,S原子最外层有6个电子 ⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS。
A.②⑤ B.①② C.①②④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:选择题
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A.自来水 B.0.5mol·盐酸 C.0.5mol·醋酸 D.0.5mol·氯水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(B类)试卷(解析版) 题型:选择题
可以证明可逆反应N2 + 3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其它条件不变时,混合气体平均相对分子质量不再改变;④保持其它条件不变时,体系压强不再改变;⑤NH3、N2、H2的体积分数都不再改变;⑥恒温恒容时,混合气体的密度保持不变;⑦正反应速率v(H2) = 0.6 mol/(L·min),逆反应速率v(NH3) = 0.4 mol/(L·min)
A.全部 B.①③④⑤ C.②③④⑤⑦ D.③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏江阴高一上暑期学习反馈(开学检测)化学试卷(解析版) 题型:选择题
苹果汁中含有Fe2+,它是人们喜欢的一种补铁饮料,现榨的苹果汁在空气中会由淡绿色逐渐变为棕黄色。若榨汁时加入维生素C,可以防止这种现象发生。这说明维生素C具有( )
A.还原性 B.氧化性 C.碱性 D.酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com