
����Ŀ�����������£���һԪ��HA����Һ��KOH��Һ�������ϣ����Ի�Ϻ���Һ������仯����ʵ���������±���
ʵ����� | ��ʼŨ�ȣ���mol��L��1�� | ��Ӧ����Һ��pH | |
c��HA�� | c��KOH�� | ||
�� | 0.1 | 0.1 | 9 |
�� | x | 0.2 | 7 |
��ش�
��1��HA��Һ��KOH��Һ��Ӧ�����ӷ���ʽΪ________��
��2��ʵ������Ӧ�����Һ����ˮ�������c��OH������________mol��L��1��x________0.2mol��L��1����������������������������
��3�����й���ʵ������Ӧ�����Һ˵������ȷ����________������ĸ����
a����Һ��ֻ����������ƽ��
b����Һ�У�c��A������c��HA����0.1mol��L��1
c����Һ�У�c��K������c��A������c��OH������c��H����
������֪2H2��g����O2��g����2H2O��1�� ��H����572kJ��mol��1��ij����ȼ�ϵ�������ɶ��ʯī��Ϊ�缫��KOH��ҺΪ�������Һ��
��4��д���õ�ع���ʱ�����ĵ缫��Ӧʽ________��
��5����������ȼ�ϵ��ÿ�ͷ�228.8kJ����ʱ��������1molҺ̬ˮ����õ�ص�����ת����Ϊ________��
���𰸡� HA��OH����A����H2O 1��10��5 �� a H2��2OH����2e����2H2O 80��
������������(1)��Ũ�Ⱥ͵������HA��Һ��KOH��Һ��Ϻ���Һ�Լ��ԣ�˵��HAΪ���ᣬ��HA��Һ��KOH��Һ��Ӧ�����ӷ���ʽΪHA+OH����A����H2O��
(2)ʵ������Ӧ�����Һ��pH=9����Һ��OH-��Դ��ˮ����ˮ�������c(OH��)��![]() mol��L��1=1��10-5mol��L��1��������Ϊǿ�ᣬ�������Ũ�Ȼ��ʱpH=7����HAΪ���ᣬ�������Ũ�Ȼ����Һ��pH����7����Ϊ��֤pH=7��Ӧʹ��Ũ��Ӧ�ô���0.2mol/L��
mol��L��1=1��10-5mol��L��1��������Ϊǿ�ᣬ�������Ũ�Ȼ��ʱpH=7����HAΪ���ᣬ�������Ũ�Ȼ����Һ��pH����7����Ϊ��֤pH=7��Ӧʹ��Ũ��Ӧ�ô���0.2mol/L��
(3)a��ʵ������Ӧ����Һ��ֻ����HA�ĵ��롢ˮ�ĵ��뼰A-��ˮ��ƽ�⣬��a����b����Ũ�ȴ���0.2mol/L�����������غ�c(A��)��c(HA)��0.1mol��L��1����b��ȷ��c����Һ��pH=7����ϵ���غ�ɵ�c(K��)��c(A��)��c(OH��)��c(H��)����c��ȷ����Ϊa��
����(4)������ȼ�ϵ�صĸ����Ϸ���ʧ���ӵ�������Ӧ���� H2��2OH����2e����2H2O��
(5)H2(g)+![]() O2(g)=H2O(l)��H=-286KJmoL-1������ȼ�ϵ���ͷ�228.8kJ����ʱ������1molҺ̬ˮ���õ�ص�����ת����Ϊ
O2(g)=H2O(l)��H=-286KJmoL-1������ȼ�ϵ���ͷ�228.8kJ����ʱ������1molҺ̬ˮ���õ�ص�����ת����Ϊ![]() ��100%=80%��
��100%=80%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A�������ӵ�������ȷֵӦΪ6.02��1023mol��1
B����״���£�17g���������Ϊ22.4L/mol
C�����³�ѹ�����£�3.6gH2O������ԭ����Ϊ0.4NA
D��Ũ��Ϊ0.1 mol/LNa2CO3��Һ�У�Na+��Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���ڷ��ȷ�Ӧ����
A. Ũ����ϡ�� B. ʯ��ʯ���ȷֽ�
C. ̼�۲���ȫȼ�� D. ���������������Ȼ�茶����Ͻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���A��B��C��D��E�����л�����й���Ϣ��
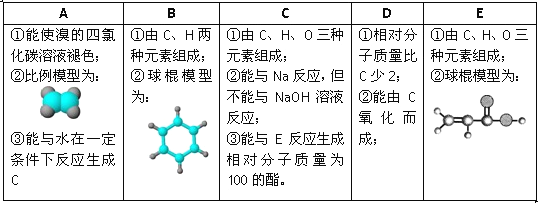
���ݱ�����Ϣ�ش��������⣺
(1)A��E�У�����������_______(����ĸ)��д��A����ˮ��Ӧ�Ļ�ѧ����ʽ_____________��
(2)A�����������ӳɷ�Ӧ�����ɷ���F����F�ڷ�����ɺͽṹ�����Ƶ��л�����һ����(�׳ơ�ͬϵ�)�����Ǿ�����ͨʽ_______����n=________ʱ�������л��↑ʼ����ͬ���칹�塣
(3)B���������_____________(�����)��
����ɫ��ζҺ�� ���ж� �۲�����ˮ ���ܶȱ�ˮ��
���κ������²���������Ӧ��ʹ���Ը��������Һ����ˮ����ɫ
(4)д����Ũ���������£�B��Ũ���ᷴӦ�Ļ�ѧ����ʽ��_________________��
(5)C��E��Ӧ��������Է�������Ϊ100�������÷�Ӧ����Ϊ_____________���仯ѧ����ʽΪ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е����ӣ�������Һ�й�����ǣ�������
A.K+��H+��SO42����OH��
B.Na+��Ca2+��CO32����NO3��
C.Na+��H+��Cl����CO32��
D.Na+��Cu2+��Cl����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƻ��֭������ϲ�����ϣ����ڴ������к���Fe2+ �� ��ե��ƻ��֭�ڿ����л��ɵ���ɫ��Ϊ�ػ�ɫ����ե֭ʱ����ά����C������Ч��ֹ��������������˵��ά����C���У�������
A.������
B.��ԭ��
C.����
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ˮ��Һ���Դ������Ӵ��ڵ��ǣ� ��
A��H2 B��H2O C��CaCO3 D��CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ϩ������ƽ��ṹ�����1,2������ϩ�����γ����ֲ�ͬ�Ŀռ��칹�塣���и������У����γ������������ֿռ��칹�����( )
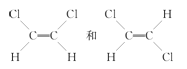
A��1����ϩ B����ϩ C��2������2����ϩ D��2���ȣ�2����ϩ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com