
取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压条件下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是( )
A.1∶1∶2 B.2∶1∶3 C.6∶3∶2 D.3∶2∶1
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
工业上生产硫酸的流程图如下:

请回答下列问题:
(1)早期生产硫酸以黄铁矿为原料,但现在工厂生产硫酸以硫黄为原料,理由是________________________________________________________________________。
(2)在气体进入催化反应室前需净化的原因是_________________________ ________
________
_____________________ ___________________________________________________。
___________________________________________________。
(3)在催化反应室中通常使用常压,在此条件下SO2的转化率为90%。但是部分发达国家采取高压条件下制取SO3,采取加压措施的目的除了加快反应速率外,还可以____________________________,从而提高生产效率。
(4)工业生产中常用氨—酸法进行尾气脱硫,以达到消除污染,废物利用的目的。用化学方程式表示其反应原理:____________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)除硫酸工业外,还有许多工业生产。下列相关的工业生产流程中正确的是________。
A.海水提溴:海水浓缩热空气或水蒸气溴蒸气碱液吸收液溴
B.海水提镁:海滩贝壳石灰水MgO熔化电解镁
C.工业制硝酸:空气NO2水吸收硝酸—→尾气处理
D.工业合成氨:天然气一定条件下氢气合成塔过量氮气NH3、H2、N2水冷分离氨
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
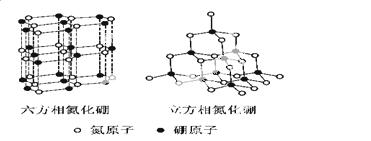
⑴基态硼原子的电子排布式为 。
⑵ 关于这两种晶体的说法,正确的是 (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大 b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键 d.两种晶体均为分子晶体
⑶六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石墨相似却不导电,原因是 。
⑷立方相氮化硼晶体中,硼原子的杂化轨道类型为 。该晶体的天然矿物在青藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
⑸NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有 mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。
请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为________,第一电离能最小的元素是________(填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是________(填化学式),呈现如此递变规律的原因是___________________。
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为________。另一种的晶胞如图二所示,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为________________________________________________g·c m-3(保留两位有效数字)。(
m-3(保留两位有效数字)。(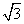 =1.732)
=1.732)
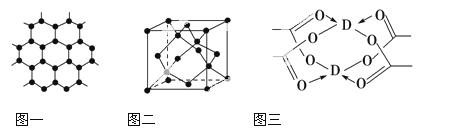
(4)D元素形成的单质,其晶体的堆积模型为________,D的醋酸盐晶体局部结构如图三,该晶体中含有的化学键是________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是________。请写出上述过程的离子方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2Fe + 3Br2 = 2FeBr3,Fe2+的还原性大于Br-。现有16.8 g铁和0.3 mol Br2反应后加入水得到澄清溶液后,通入a mol Cl2。下列叙述不正确的是
A.当a = 0.1时,发生的反应为2Fe2++Cl2=2Fe3++2Cl-
B.当a = 0.45时,发生的反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C.若溶液中Br-有一半被氧化时, c(Fe3+): c(Br-):c(Cl-) =1:1:3
D.当0<a<0.15时,溶液中始终满足2c(Fe2+)+3c(Fe3+)+c(H+)=c(Cl-)+c(Br-)+ c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强从大到小的顺序是
A.p(Ne) >p(H2) >p(O2) B.p(O2) >p(Ne) >p(H2)
C.p(H2) >p(O2) >p(Ne) D.p(H2) >p(Ne) >p(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有关知识的理解正确的是( )
A.物质的量是物质所含微粒的数量
B.1摩尔氧气的质量等于NA个O2分子的相对分子质量之和
C.阿伏加德罗常数是人们规定的数,没有单位
D.当H2的摩尔质量以g·mol-1为单位时,在数值上与H2的相对分 子质量相等
子质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
1.28 g某气体含有的分子数目为1.204×1 022,则该气体的摩尔质量为( )
022,则该气体的摩尔质量为( )
A.64 g B. 64
C.64 g/mol D.32 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家在《自然》杂志上报告,他们用DNA制造出了一种臂长只有7 nm的纳米级镊子,以便能够钳起分子或原子并对它们随意组合。下列分散系中的分散质的粒子直径和这种纳米级镊子具有相同数量级的 是( )
是( )
A.溶液 B.胶体
C.悬浊液 D.乳浊液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com