
科目:高中化学 来源:不详 题型:单选题
 NH4++NH2—,NH4+的平衡浓度为1×10-15mol·L-1,下列说法错误的是( )
NH4++NH2—,NH4+的平衡浓度为1×10-15mol·L-1,下列说法错误的是( )| A.在液氨中加入NaNH2,可使液氨的离子积变大 |
| B.在液氨中加入NH4Cl,液氨的离子积不变 |
| C.此温度下液氨的离子积K为1×10-30 |
| D.在液氨中加入金属钠可能有NaNH2生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2SO2 (g)+O2 (g) 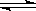 2SO3 (g) ;△H<0 2SO3 (g) ;△H<0 |
B.H2 (g)+I2 (g) 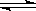 2HI (g) ;△H>0 2HI (g) ;△H>0 |
C.4NH3 (g)+5O2 (g) 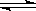 4NO(g)+6H2O (g) ;△H<0 4NO(g)+6H2O (g) ;△H<0 |
D.C (s)+H2O (g) 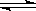 CO (g)+H2 (g) ;△H>0 CO (g)+H2 (g) ;△H>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应:2CO(g)+2NO(g) |
| B.0.1mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小 |
| C.为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 |
D.反应:2A(g)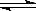 B(g)+2C(g),增大压强反应速率加快,A的转化率减小 B(g)+2C(g),增大压强反应速率加快,A的转化率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| l | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )
2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )| A.1mol·l-1 | B.0.1mol·l-1 | C.0.9mol·l-1 | D.0.2mol·l-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。H2应从电解池的________ (填电极名称)通入;其中b电极的电极反应方程式为________。
。H2应从电解池的________ (填电极名称)通入;其中b电极的电极反应方程式为________。
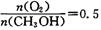 时,制备反应分两步进行,其中一步是
时,制备反应分两步进行,其中一步是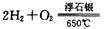
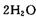 ,则另一步是____________ (写化学方程式)。
,则另一步是____________ (写化学方程式)。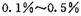 的HCHO可用于杀菌消毒,其原因是________。
的HCHO可用于杀菌消毒,其原因是________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
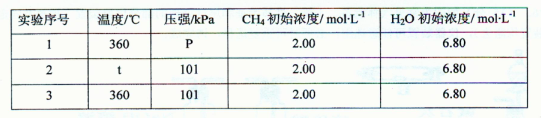
 CO(g)+3H2(g);△H=+206.lkJ·mol-l。
CO(g)+3H2(g);△H=+206.lkJ·mol-l。
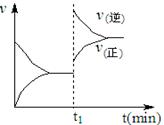
| A.v(正)>v(逆) | B.v(正)<v(逆) |
| C.v(正)=v(逆) | D.无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com