
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸。
 (1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为: ,该反应在 中进行(填仪器名称)。
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为: ,该反应在 中进行(填仪器名称)。
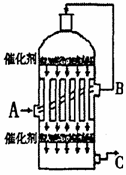
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂
且有热交换器的 (填仪器名称)中进行反应。在如图所示的装置中, C处流出的气体有 ;SO3进入 (填仪器名称)用 吸收,得到浓硫酸或发烟硫酸。
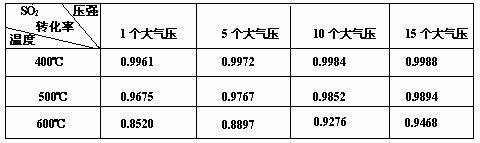
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下
表信息,结合工业生产实际,选择最合适的生产条件是 。
 |
(4)现在欲提高SO2的反应速率和转化率,下列措施可行的是 。
A、向装置中通入氮气且保持体积不变 B、向装置中通入氧气且保持体积不变
C、添加更多的催化剂 D、降低温度,及时转移SO3
(5)由吸收塔排出的尾气中有SO2的含量如果超过500μL/ L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式 。
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 含有非极性键的分子不一定是共价化合物。
B. 分子间作用力比化学键弱得多,但它对物质的熔点、沸点有较大的影响,而对溶解度无影响。
C. 根据π键的成键特征判断C=C键能是C—C键能的2倍。
D. H2O中心原子采取sp杂化。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.将锌粒投入Cu(NO3)2溶液 D.碳酸氢钠固体加热至没有气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
把铝、铁混合物1.1 g溶于200 mL 5 mol/L盐酸中,反应后盐酸的浓度变为4.6 mol/L (溶液体积变化忽略不计)。
(1)反应中消耗HCl的物质的量 mol。
(2)该混合物中铝的质量为 g,铁的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
下列有关叙述正确的是
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A. ΔH<0、ΔS>0的反应在任何温度下都能自发进行
B. NH4HCO3(s) NH3 (g)+H2O(g)+CO2(g) ΔH=+185.57 kJ·mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
NH3 (g)+H2O(g)+CO2(g) ΔH=+185.57 kJ·mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
C. 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D. 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
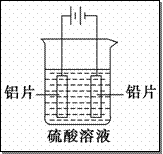 铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的 氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是( )。
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的 氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是( )。
A.电解时电子从电源负极→导线→铝极,铅极→导线→电源正级
B.在电解过程中,H+向阳极移动,SO42-向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com