


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源:不详 题型:实验题
 ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
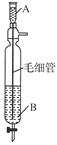
| A.A为浓盐酸,B为浓硫酸,制得HCl气体 |
| B.A为浓氨水,B为浓氢氧化钠溶液,制得NH3 |
| C.A为浓醋酸,B为浓硫酸,制得CH3COOH |
| D.A为浓HI溶液,B为浓硫酸,制得HI气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
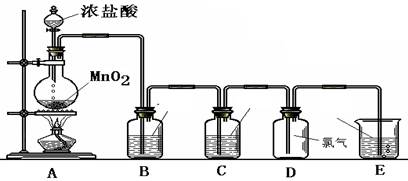
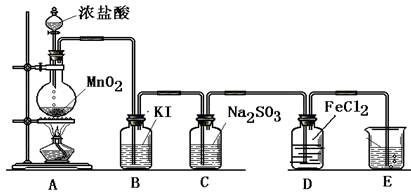
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
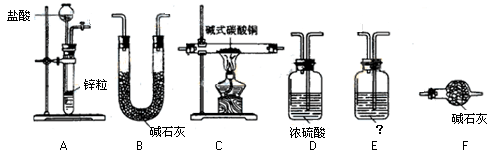
 置用代号表示):
置用代号表示):
 室制二氧化碳时,应选用
室制二氧化碳时,应选用 的发生装置是__ __;检验二氧化碳气体可选用D装
的发生装置是__ __;检验二氧化碳气体可选用D装 置,其装置中盛放的试剂一般是__ __。
置,其装置中盛放的试剂一般是__ __。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
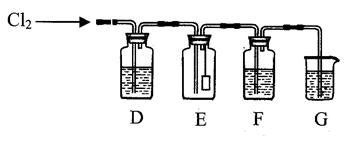
 方程式 。
方程式 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com