
 ��ͬѧ���Ѿ�ѧϰ��ͬλ�ء�ͬϵ�ͬ�������塢ͬ���칹�壬����������Щ�����������г��˼������ʣ��������ʵ������д�±���
��ͬѧ���Ѿ�ѧϰ��ͬλ�ء�ͬϵ�ͬ�������塢ͬ���칹�壬����������Щ�����������г��˼������ʣ��������ʵ������д�±���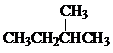 ��
��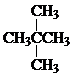
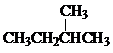 ��
��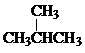
| ��� | ͬλ�� | ͬϵ�� | ͬ�������� | ͬ���칹�� |
| ��� |
| ��c |
| ��t |
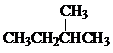 ��
��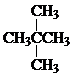 ����ʽ��ͬ�����ṹ��ͬ���ʻ�Ϊͬ���칹�壻
����ʽ��ͬ�����ṹ��ͬ���ʻ�Ϊͬ���칹�壻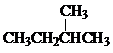 ��
��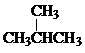 �ṹ���ƣ�����������1����CH2�����ʻ�Ϊͬϵ�
�ṹ���ƣ�����������1����CH2�����ʻ�Ϊͬϵ�| ��� | ͬλ�� | ͬϵ�� | ͬ�������� | ͬ���칹�� |
| ��� | �� | �� | �ۢ� | �٢� |
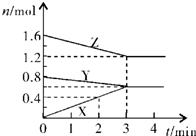
 3X���ʴ�Ϊ��Y+2Z
3X���ʴ�Ϊ��Y+2Z 3X��
3X��| ��c |
| ��t |
| ||
| 3min |


 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
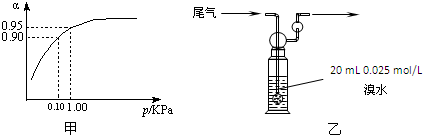
| �� �� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 2mol SO2��1mol O2 | 2mol SO3 | m mol SO2��n mol O2�� p mol SO3 |
| c��SO3��/mol?L-1 | 1.4 | 1.4 | 1.4 |
| �����仯 | �ų�a kJ | ����b kJ | ����c kJ |
| SO2��SO3��ת���� | ��1 | ��2 | 12.5% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
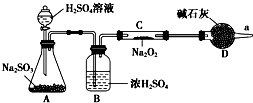 ��ijѧ������SO2���л�ԭ���ж�SO2��Na2O2��Ӧ�����������ƣ���ͬѧ���϶���Ӧ���Ƿ����������ɣ���ʹ����ͼ��ʾװ�ý���ʵ�飨AΪSO2�ķ���װ�ã�ͼ������̨��װ������ȥ����
��ijѧ������SO2���л�ԭ���ж�SO2��Na2O2��Ӧ�����������ƣ���ͬѧ���϶���Ӧ���Ƿ����������ɣ���ʹ����ͼ��ʾװ�ý���ʵ�飨AΪSO2�ķ���װ�ã�ͼ������̨��װ������ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢۢ� | B���ڢۢ� |
| C���ܢݢ� | D���٢ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com