
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是( )
A.原子半径:Z > W > R
B.对应的氢化物的热稳定性:R>W
C.W与X、W与Z形成化合物的化学键类型完全相同
D.Y的最高价氧化物对应的水化物是弱酸
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
下列有关说法正确的是
A. 含有碳元素的化合物一定是有机化合物
B. 生物柴油和柴油的主要成分不同
C. 废弃的可降解高分子材料会造成白色污染
D. 淀粉和纤维素的分子式都可表示为(C6H10O5)n,淀粉和纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里用加热正丁醇、溴化钠和浓硫酸的混合物的方法来制备1—溴丁烷,已知有关物质的性质如下:
| 熔点/℃ | 沸点/℃ | 密度/ | |
| 正丁醇 | -89.53 | 117.25 | 0.81 |
| 1—溴丁烷 | -112.4 | 101.6 | 1.28 |
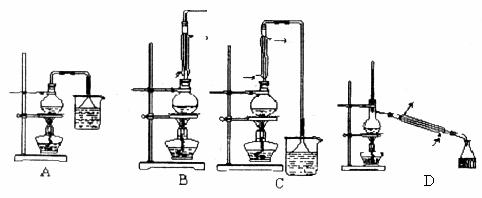
(1)生成1—溴丁烷的化学方程式为__________________。
(2)由于副反应的发生而可能产生的副产物有_______________。(至少两种,有机物用结构简式表示)
(3)为了将反应混合物中1—溴丁烷及时分离出,应选用的装置是_____________(填序号),该操作应控制的温度t2范围是_______________。
(4)在得到的1—溴丁烷的产物中出现了分层现象,某同学选择用分液的方法进行分离。在本实验分离过程中,产物应该从分液漏斗的___________(填“上口倒出”或“下口放出”)。
(5)本实验所用的正丁醇质量为20.0g,最后得到纯净的1—溴丁烷的质量为22.2g,本实验的产率约是_________(填正确答案标号)。
A. 40% B. 50% C. 60% D. 70%
查看答案和解析>>
科目:高中化学 来源: 题型:
医学研究证明,用放射性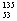 I治疗肿瘤可收到一定疗效,下列有关
I治疗肿瘤可收到一定疗效,下列有关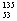 I叙述正确的是( )。
I叙述正确的是( )。
A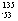 I是碘的一种同素异形体
I是碘的一种同素异形体
B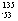 I是一种新发现的元素
I是一种新发现的元素
C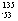 I位于元素周期表中第四周期ⅦA族
I位于元素周期表中第四周期ⅦA族
D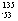 I核内的中子数与核外电子数之差为29
I核内的中子数与核外电子数之差为29
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组微粒具有相同的质子数和电子数的是( )。
A.OH-、H2O、F- B.NH3、NH 、NH
、NH
C.H3O+、CH4、HF D.HCl、F2、H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
|
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
回答下列问题:
(1)④的元素名称是 ,②在元素周期表中的位置是(周期、族)
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ;
(3)①、⑥的简单离子的半径大小关系____________________。(填化学式)
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(5)写出⑥最高价氧化物对应水化物跟同周期另一金属元素的最高价氧化物反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,11.2 L的戊烷所含的分子数为0.5NA
B.28 g乙烯所含共用电子对数目为4NA
C.1 mol甲基的电子数目为7 NA
D.现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关碱金属元素性质的叙述中,正确的是 ( )
A.碱金属的单质中,锂的还原性最强
B.K与水反应最剧烈
C.在自然界中它们无游离态存在
D.单质的熔沸点依次升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com