
| O | 2 3 |
| O | 2 4 |
| O | 2 3 |
| O | 2- 4 |
| A、①③ | B、②③ | C、③⑤ | D、④⑤ |
| 2.33g |
| 233g/mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
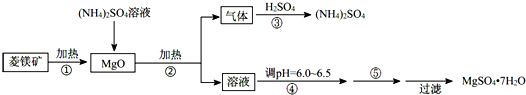
| A、①②③⑥ | B、③④⑤⑥ |
| C、②④⑤⑥ | D、①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 尿素(H2NCONH2 )可用于制有机铁肥.主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]
尿素(H2NCONH2 )可用于制有机铁肥.主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH2CH3和CH3CH2CH2CH3 |
| B、H2NCH2COOH和CH3CH2NO2 |
| C、CH3CH2COOH和CH3COOCH2CH3 |
| D、CH2=CHCH2CH3和CH2=CHCH=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
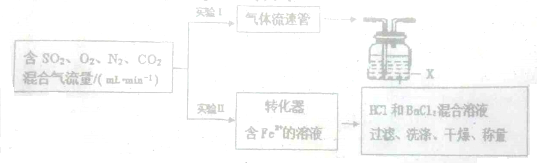
| A、Mg2+ |
| B、Fe3+ |
| C、Cl- |
| D、Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com