
| A. | 甲烷燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 铝片与盐酸反应 | D. | 氧化钙与水反应 |
分析 生成物总能量高于反应物总能量的反应属于吸热反应,根据常见的放热反应和吸热反应进行判断.若反应物的总能量大于生成物的总能量则为放热反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应、绝大多数化合反应,铝热反应;
常见的吸热反应有:个别的化合反应(如C和CO2)、绝大数分解反应、少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A.甲烷燃烧属于放热反应,生成物的总能量小于反应物的总能量,故A错误;
B.Ba(OH)2•8H2O与NH4Cl反应属于吸热反应,生成物总能量高于反应物总能量,故B正确;
C.铝与稀盐酸反应属于放热反应,生成物的总能量小于反应物的总能量,故C错误;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量,故D错误.
故选B.
点评 本题主要考查了放热反应和放热反应,题目难度不大,掌握常见的放热反应和放热反应是解题的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期主族元素从左到右,氧化物对应的水化物酸性依次增强 | |
| B. | H2O比H2S的稳定性强,是因为其分子之间存在氢键 | |
| C. | 金刚石呈正四面体网状结构、C60呈笼状结构,这两种晶体中微粒间的作用力不完全相同 | |
| D. | NH4Cl属于离子化合物,该物质中只存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | 部 分 性 质 |
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是核外电子总数的$\frac{7}{17}$ |
| Z | 第三周期原子半径最小的金属 |
| A. | 第一电离能:Y>Z | |
| B. | 离子半径:W>Z | |
| C. | X、Y形成的化合物XY4是离子化合物 | |
| D. | 工业上利用电解熔融Z的氧化物生产Z金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | 气态氢化物的稳定性:Y>W>X | |
| B. | X、Y两种元素形成的化合物只有两种 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:HF>HCl>HBr>HI | |
| B. | 稳定性:HF<HCl<HBr<HI | |
| C. | 从F2到I2,颜色逐渐加深 | |
| D. | 与氢气化合由易到难:I2>Br2>Cl2>F2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
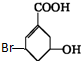
| A. | 该有机物的分子式为C7H9O3Br | |
| B. | 该有机物可使溴水褪色 | |
| C. | 该有机物可发生加成反应、消去反应、取代反应等 | |
| D. | 1mol该有机物与NaOH溶液反应时只能消耗1molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCN的电离方程式:HCN?H++CN- | |
| B. | NaCN是一种弱电解质 | |
| C. | NaCN溶液中一定存在:c(Na+)>c(CN-) | |
| D. | 0.1mol•L-1NaCN溶液中:c(CN-)+c(HCN)=0.1mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com