
| A. | 容量瓶 | B. | 分液漏斗 | C. | 干燥器 | D. | 滴定管 |
分析 测定硫酸铜晶体(CuSO4•5H2O)里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量,结合操作步骤判断使用的仪器,以此解答该题.
解答 解:测定硫酸铜晶体中结晶水含量的实验步骤为:①研磨、②称量空坩埚和装有试样的坩埚的质量、③加热、④冷却、⑤称量、⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止、⑦根据实验数据计算硫酸铜结晶水的含量,则所需仪器有:托盘天平、研钵、酒精灯、玻璃棒、坩埚、干燥器、泥三角、三角架、药匙、坩埚钳,
题中只有干燥器符合.
故选C.
点评 本题考查了硫酸铜晶体中结晶水含量测定,题目难度不大,明确操作步骤为解答关键,注意掌握常见仪器的构造及使用方法,试题侧重基础知识的考查,有利于提高学生的化学实验能力.


科目:高中化学 来源: 题型:选择题

| A. | 该物质的结构简式为 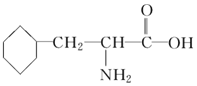 | |
| B. | 该物质可以发生加成反应 | |
| C. | 该物质既可以与强酸反应,但不可以与强碱反应 | |
| D. | 该物质不可以聚合成高分子物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去热水瓶中的水垢 | |
| B. | 用米汤检验加碘盐中的碘酸钾(KIO3) | |
| C. | 向Al2(SO4)3溶液中加过量NaOH溶液,制Al(OH)3 | |
| D. | 向稀H2SO4催化水解后的麦芽糖溶液中直接加入新制Cu (OH)2悬浊液,检验水解产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
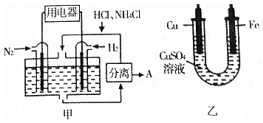 如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.| A. | 通入H2-极与图乙中的铜电极相连 | |
| B. | 电池工作一段时间后,溶液pH减少1 | |
| C. | 当消耗0.025molN2时,则铁电极增重1.6g | |
| D. | 通入N2-端的电极反应式为:N2+8H++6e-═2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.lmol的Na2O2含阴阳离子总数为0.4NA | |
| B. | 32g硫与足量金属铜反应转移电子数为NA | |
| C. | 标准状况下,11.2LNO与11.2LO2混合后其原子总数为2NA | |
| D. | 1LpH=1的硫酸溶液中,含有0.2NA个H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
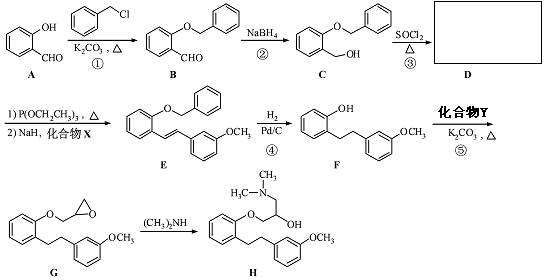

 .
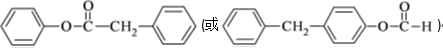
.
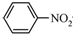 $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$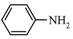 .化合物
.化合物  是合成抗癌药物美法
是合成抗癌药物美法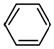 和
和 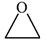 为原料制备该化合物的合成路线流程图(无机试剂任
为原料制备该化合物的合成路线流程图(无机试剂任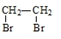
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com