
分析 根据n=$\frac{m}{M}$计算出10.6g Na2CO3的物质的量,然后可得出含有钠原子、碳原子、氧原子的物质的量;碳酸钠含有的电子数=质子数=52,根据N=nNA计算出含有的碳原子、氧原子、电子和质子数.
解答 解:10.6g Na2CO3的物质的量为:n(Na2CO3)=$\frac{10.6g}{106g/mol}$=0.1mol,0.1mol Na2CO3中含有钠原子的物质的量为:n(Na)=0.1mol×2=0.2mol;含有碳原子的物质的量为:n(C)=n(Na2CO3)=0.1mol,数目为0.1NA;含有O原子的物质的量为:n(O)=0.1mol×3=0.3mol,数目为0.3NA;含有的电子、质子的物质的量相等,都为0.1mol×52=5.2mol,数目为5.2NA,
故答案为:0.2;0.1NA;0.3NA;5.2;5.2NA.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量之间的关系即可解答,试题培养了学生的化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸溶液与氢氧化钡溶液混合:Ba2++SO42-=BaSO⒋↓ | |
| B. | 稀硫酸中加入铜片:Cu+2H+=Cu2++H2↑ | |
| C. | 氧化铜溶于盐酸:O2-+2H+=H2O | |
| D. | 二氧化碳通入足量澄清石灰水:Ca2++2OHˉ+CO2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L稀硫酸中含有硫酸根数目为0.1NA | |
| B. | 9g H2O中含有H数目为1mol | |
| C. | 2.4g金属镁与足量的盐酸反应,生成氢分子数目为2NA | |
| D. | 1mol NH4+中含有电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
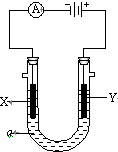 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com