
有七种物质:①甲烷、②苯、③聚乙烯、④聚异戊二烯、⑤2﹣丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
|
| A. | ③④⑤⑧ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦ |
考点:
有机物的结构和性质.
专题:
有机物的化学性质及推断.
分析:
既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的有机物,应含有不饱和碳碳键或醛基,以此解答该题.
解答:
解:①甲烷为饱和烃,与酸性高锰酸钾或溴水都不反应,故①错误;
②苯结构特殊、性质稳定,与酸性高锰酸钾或溴水都不反应,故②错误;
③聚乙烯不含不饱和键,不能与酸性高锰酸钾或溴水反应,故③错误;
④聚异戊二烯含有碳碳双键,可与酸性高锰酸钾或溴水反应,故④正确;
⑤2﹣丁炔含有碳碳三键,可与酸性高锰酸钾或溴水反应,故⑤正确;
⑥环己烷不含不饱和键,不能与酸性高锰酸钾或溴水反应,故⑥错误;
⑦环己烯含有碳碳双键,可与酸性高锰酸钾或溴水反应,故⑦正确.
故选B.
点评:
本题考查有机物的结构和性质,题目难度不大,注意常见有机物官能团的性质,把握与酸性高锰酸钾或溴水反应的物质.


科目:高中化学 来源: 题型:
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol•L﹣1的一元酸HA与b mol•L﹣1一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
|
| A. | a=b |
|
| B. | 混合溶液的pH=7 |
|
| C. | 混合溶液中,c(H+)= |
|
| D. | 混合溶液中,c(H+)+c(B﹣)=c(OH﹣)+c(A﹣) |
查看答案和解析>>
科目:高中化学 来源: 题型:
C和CuO在高温下反应可能生成Cu、Cu2O、CO2、CO.现将1g碳粉跟8g CuO混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为1.1g,残余气体在标准状况下的体积为560mL.下列说法错误的是()
A. 在硬质试管中隔绝空气高温加热固体混合物时,有0.6 g碳参加了反应
B. 试管中发生的所有氧化还原反应共转移电子0.15 mol
C. 反应后试管中剩余的固体混合物的总质量为7.2 g
D. 反应生成铜和氧化亚铜的总物质的量为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g) 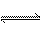 B(g)+C(g)反应的平衡常数和温度的关系如下:
B(g)+C(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ | 700 | 800 | 900 | 1000 |
| 平衡常数 | 0.4 | 0.9 | 1.0 | 1.6 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0,△S 0(填“<”“ >”“ =”)
(2)900℃时,向一个0.5 L的密闭容器中充入6mol的A,如反应初始5s内A的平均反应速率v(A)=0.4 mol·L-1·s-1。则5s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 。保持温度和体积不变,再向容器中充入4mol的A,则重新达到平衡时A的转化率为
(3)700℃时反应C(g)+B(g) A(g)的平衡常数的值为
A(g)的平衡常数的值为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 卤代烃在NaOH存在下水解生成的有机物都是醇 |
|
| B. | 所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
|
| C. |
|
|
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于石油的说法不正确的是( )
A.石油中主要含C、H两种元素
B.石油主要是由各种烃组成的混合物
C.石油有固定的沸点,故可分馏
D.石油的分馏产物仍是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
在A、B两支大试管中分别依次加入苯、H2O,再用长颈漏斗小心加入CCl4。两试管中都明显分为三层,将A试管振荡后静置(已知苯的密度小于水的密度而四氯化碳的密度大于水的密度)。
(1)溶液可分为________层,原因是________________________________。
(2)不用实验验证你能否判断出哪一层是水层_________,若能,判断的依据是________________________________________________________________________
(若不能,此问可不回答)。
(3)请你设计简单实验验证哪一层是水层: _________________________________
________________________________________________________________________。
(4)用长颈漏斗向B试管中的水层小心加入少量浓溴水,静置一段时间,试管中的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强,如下表所示:
含氧酸酸性强弱与羟基氧原子数的关系
|
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,
H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构
简式分别为① ,② 。
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
① ,② 。
(3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况: ,
写出化学方程式:_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com