
| A. | 异丁烷的所有原子都位于同一平面上 | |
| B. | 苯和溴水反应制取溴苯属于加成反应 | |
| C. | 糖类在酸性条件下水解产物均为葡糖糖 | |
| D. | 乙基环己烷的一溴代物有6种 |
分析 A.饱和烃中C为四面体构型;
B.苯不含碳碳双键,与溴水不反应;
C.单糖不能水解,且水解后不一定生成葡萄糖;
D.乙基环己烷的结构中含6种H.
解答 解:A.异丁烷( )结构中存在甲基,不可能所有原子都共面,故A错误;
)结构中存在甲基,不可能所有原子都共面,故A错误;
B.苯和溴水不能发生加成反应,苯和液溴在FeBr3催化下能生成溴苯,故B错误;
C.不是所有的糖水解产物都是葡萄糖,如蔗糖水解时果糖和葡萄糖都会生成,故C错误;
D.乙基环己烷( )有6种不同类型的氢,故一溴代物有6种,故D正确;
)有6种不同类型的氢,故一溴代物有6种,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题
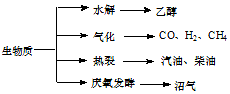 生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 不易溶于水,易溶于苯等有机溶剂 | B. | 是芳香烃,也是苯的同系物 | ||
| C. | 能发生聚合反应,其产物可表示为 | D. | 分子中所有碳原子一定在同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,在pH=6的硫酸铝溶液中,由水电离出的c(OH-)=10-6mol/L | |
| B. | 浓度为0.1mol•L-1的NaHCO3溶液:c(H2CO3)>c(CO32-) | |
| C. | 25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 | |
| D. | 向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素不能互称同分异构体 | |
| B. | 油脂在碱性条件下的水解反应成为皂化反应 | |
| C. | 向鸡蛋清溶液中加入NaCl(s)时,因蛋白质变性致溶液变浑浊 | |
| D. | 使用酸性K2Cr2O7检验酒驾的过程中,乙醇表现还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )
常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )| A. | 该Na2CO3溶液的浓度为0.001mol/L | |
| B. | 在pH=7时,c(Na+)>c(Cl-) | |
| C. | 在pH=6时,c(Na+)>c(CO32-)>c(HCO3-) | |
| D. | c→d发生的主要离子反应为:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | 碳酸钡(硫酸钡) | 饱和碳酸钠溶液 | 搅拌、过滤 |
| B | CO2(HCl) | 饱和碳酸钠溶液 | 洗气 |
| C | FeCl3(FeCl2) | 足量铁粉 | 搅拌、过滤 |
| D | HCl(Cl2) | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com