
分析 (1)物质导电的条件:存在自由电子或者自由移动的离子;
(2)在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
(3)非电解质是在水溶液里和熔融状态下都不能导电的化合物,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等).
解答 解:①食盐水含有自由移动离子,导电,属于混合物,不是电解质,也不是非电解质;
②二氧化碳不含有自由电子和自由移动离子,不导电,水溶液里和熔融状态下都不能导电,属于非电解质;
③盐酸含有自由移动离子,导电,属于混合物,不是电解质,也不是非电解质;
④蔗糖不含有自由电子和自由移动离子,不导电,水溶液里和熔融状态下都不能导电,属于非电解质;
⑤熔融的硫酸钾含有自由移动的离子,能够导电,属于电解质;
⑥氧气不含有自由电子和自由移动离子,不导电,属于单质,不是电解质,也不是非电解质;
⑦液体醋酸,不含有自由电子和自由移动离子,不导电,水溶液里能够导电,属于电解质;
⑧熔融的硫酸钾含有自由移动的离子,能够导电,属于电解质; ⑧金属铜含有自由电子,导电,属于单质,不是电解质,也不是非电解质;
⑨碳酸氢钠固体不含有自由电子和自由移动离子,不导电,水溶液里和熔融状态下能导电,属于电解质;
⑩氢氧化钠固体不含有自由电子和自由移动离子,不导电,在水溶液里或熔融状态下能导电,是电解质;
(1)根据分析可知,以上物质能导电的是:①③⑤⑧,
故答案为:①③⑤⑧;
(2)以上物质属于电解质的是:⑤⑦⑨⑩,
故答案为:⑤⑦⑨⑩;
(3)以上物质属于非电解质的是:②④,
故答案为:②④.
点评 本题考查了电解质与非电解质的判断,题目难度不大,明确电解质、非电解质的概念为解答关键,注意掌握溶液导电性的条件,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤炭经气化、液化和干馏等处理后,可转化为清洁能源 | |
| B. | “绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿的酒,在酿酒的过程中,葡萄糖发生了水解反应 | |
| C. | 地沟油和矿物油的主要化学成分相同 | |
| D. | 聚氯乙烯可以用作食品包装袋 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
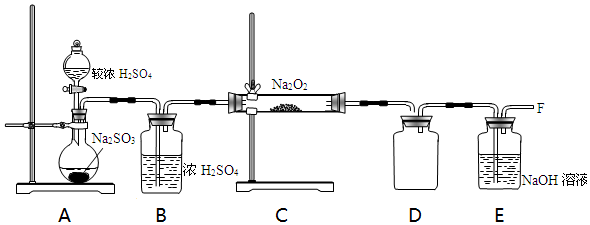
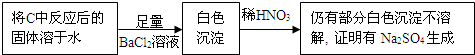
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量吸收液于试管中滴加BaCl2溶液至过量 | 白色浑浊 | 吸收液中存在SO32-和SO42- |
| 取步骤I中白色沉淀于试管中,加入过量的稀盐酸 | 固体部分溶解,产生气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
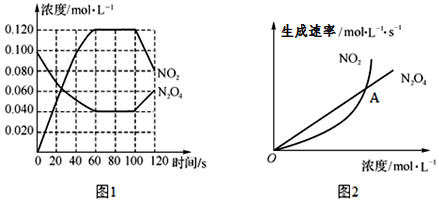
| A. | a+b+c=0 | B. | c=2a | C. | a>b | D. | c=a+b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol/L的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) | |
| B. | 常温下,将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸需加的水多 | |
| C. | 常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) | |
| D. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com