
【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
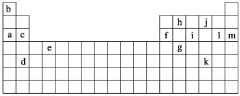
下列______(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
【答案】①
【解析】
根据元素周期表中元素的分布知识,可以知道a是Na,b是H ,c是Mg,d是Sr,e是Ti,f是Al g是Ge,h是C, j是O, i是S ,k是Sb , l是Cl ,m是Ar。金属是电的良导体,石墨碳棒是电的,良导体,金属有Na、Mg、Sr、T i、Al锗是半导体进行分析。
①根据元素周期表可知:a为Na、c为Mg、它们都属于金属单质能导电,h为C属于非金属,但其单质石墨能够导电,故①符合题意;
②根据元素周期表可知:b为H,g为As,k为碲,都属于非金属元素,形成的单质不能导电,故②不符合题意;
③根据元素周期表可知:c为Mg属于金属单质能导电,h为B,l为Cl,形成非金属单质不能导电,故③不符合题意;
④根据元素周期表可知:d为锶,e为钛,f为铝,他们都是金属,形成金属单质能导电,故④符合题意;
答案:①④。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用碱性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法中正确的是( )

A.燃料电池工作时负极反应为:H2=2H++2e-
B.若要实现铁上镀铜,则a极是铁,b极是铜
C.若要实现电解精炼粗铜,则a极发生氧化反应,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下,当电池中消耗H222.4L(标准状况)时,a极析出铜64g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去CuCl2酸性溶液中的FeCl3,加热搅拌的条件下加入一种试剂,然后再加入适量盐酸,该试剂不能是( )
A.Cu(OH)2B.CuCO3C.NaOHD.CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向容器中同时通入甲烷、氧气和水蒸气三种气体,发生的化学反应有:
反应过程 | 化学方程式 | 焓变
| 活化能
|
甲烷氧化 |
|
|
|
|
|
| |
蒸汽重整 |
|
|
|
|
|
|
(1)已知:![]() ,则
,则![]() 燃烧热
燃烧热![]() _____。
_____。
(2)在初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,原因可能是______。
(3)恒温恒压体系(温度为![]() ,压强为
,压强为![]() ),反应
),反应![]() 达到平衡时,各气体的物质的量均为
达到平衡时,各气体的物质的量均为![]() ,用某气体组分
,用某气体组分![]() 的平衡分压(分压=总压×物质的量分数)代替物质的量浓度
的平衡分压(分压=总压×物质的量分数)代替物质的量浓度![]() 也可表示平衡常数(记作
也可表示平衡常数(记作![]() )。则:
)。则:
①平衡常数![]() ___。
___。
②再向容器中瞬时同时充入![]() 、
、![]() 、
、![]() 、
、![]() ,此时
,此时![]() (正)____
(正)____![]() (逆)(填“>”“<”或“=”)
(逆)(填“>”“<”或“=”)
③恒温恒容条件下,将![]() 、
、![]() 、
、![]() 、
、![]() 按照体积比
按照体积比![]() 投料,能判断反应
投料,能判断反应![]() 达到平衡状态的是____。
达到平衡状态的是____。
A 密度保持不变 B ![]() 体积分数保持不变
体积分数保持不变
C 平均摩尔质量保持不变 D ![]() 和
和![]() 的比保持不变
的比保持不变
E ![]() 断裂的同时,有
断裂的同时,有![]() 断裂
断裂
(4)向绝热恒容密闭容器中通入![]() 和
和![]() 使反应
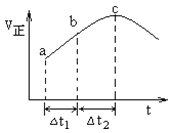
使反应![]() 达到平衡,正反应速率随时间变化的示意图如图所示。图中
达到平衡,正反应速率随时间变化的示意图如图所示。图中![]() 点反应是否达到平衡,说明理由_____。
点反应是否达到平衡,说明理由_____。
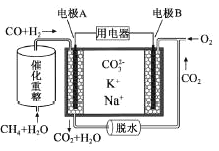
(5)利用重整反应![]() ,设计一种熔融碳酸盐燃料电池,原理示意图,电极
,设计一种熔融碳酸盐燃料电池,原理示意图,电极![]() 上发生的电极反应为______。
上发生的电极反应为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式硫酸铁[Fex(OH)y(SO4)z](其中Fe元素为+ 3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量Al2O3、Fe2O3)生产碱式硫酸铁的工艺流程如下:
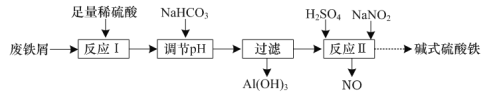
下列说法正确的是
A.x、y、z一定符合关系式:x=y=z
B.“过滤”所得滤液中只含溶质FeSO4
C.“反应Ⅰ”中包含的反应类型有置换反应、化合反应和复分解反应
D.在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若有11.2 L(标准状况)的O2参与反应,则相当于节约2 mol NaNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃条件下,向![]() 的盐酸中不断通
的盐酸中不断通![]() ,该过程中水电离出的氢离子浓度
,该过程中水电离出的氢离子浓度![]() 水
水![]() 与通入
与通入![]() 的物质的量关系如图,下列说法不正确的是( )。
的物质的量关系如图,下列说法不正确的是( )。
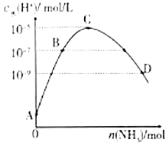
A.![]() 点的纵坐标为
点的纵坐标为![]()
B.![]() 点溶液中
点溶液中![]()
C.![]() 点溶液中
点溶液中![]()
D.![]() 点溶液的
点溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种硫化矿(含45%SiO2、20.4% Al2O3、30%FeS和少量GeS2等)制取盆景肥料NH4Fe(SO4)2及铝硅合金材料的工艺流程如下 :
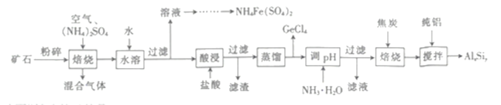
(1)“矿石”粉碎的目的是_____________________ 。
(2)“混合气体”经过水吸收和空气氧化能再次利用。
①“焙烧”时,GeS2发生反应的化学方程式为____________________。
②“混合气体”的主要成分是_______________ (填化学式).
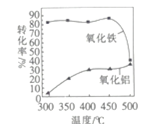
③FeS焙烧产生的Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,该反应的化学方程式为_______________。 Al2O3也能发生类似反应.这两种氧化物转化为硫酸盐的转化率与温度的关系如图,上述流程中最适宜的“焙烧” 温度为_____________________。
(3)GeCl4的佛点低,可在酸性条件下利用蒸馏的方法进行分离,酸性条件的目的是_________。
(4)用电解氧化法可以增强合金 AlxSiy的防腐蚀能力,电解后在合金表面形成致密、耐腐蚀的氧化膜(主要成分为Al2O3), 电解质溶液为 H2SO4-H2C2O4混合溶液,阳极的电极反应式为______________________。
(5)假设流程中SiO2 损失了20%,Al2O3 损失了25%,当投入1 t硫化矿,加入了54kg纯铝时,铝硅合金中x:y=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com