
【题目】Cyrneine A对治疗神经系统疾病有着很好的疗效。可用香芹酮经过多步反应合成: ,下列说法不正确的是( )
,下列说法不正确的是( )
A.香芹酮的分子式为C10H14O
B.Cyrneine A可以发生加成反应、消去反应和氧化反应
C.香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色
D.与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物共有3种
【答案】D
【解析】
试题分析:A、先由香芹酮的键线式、有机物中碳氢氧原子的成键特点可知,其分子式为C10H14O,再由分子式中碳原子数-氢原子数/2+1可知其不饱和度(Ω)为10-14/2+1=4,然后由结构简式中2个C=C、1个C=O和1个环可知其不饱和度为2+1+1=4,两种算法所得结果相同,A正确;B、由Cyrneine A的键线式可知它含有碳碳双键和醛基(能发生加成反应)、羟基且其相连碳原子连有2个C-H键(能发生消去反应),上述三种官能团及烃基能发生氧化反应或燃烧,B正确;C、香芹酮和Cyrneine A均含有碳碳双键,均能被酸性高锰酸钾溶液氧化,C正确;D、与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物,说明分子中含有酚羟基,如果苯环上只有2个取代基,则另一个是-C(CH3)3(才能满足分子中有4种不同化学环境的氢原子),且位于酚羟基的对位;如果含有3个取代基,则另外2个都是乙基,且位于酚羟基的邻位或间位;如果含有4个取代基,则另外3个都是甲基,且2个位于酚羟基的邻位、1个位于对位,或者2个位于酚羟基的对位、1个位于邻位,因此可能的结构简式超过3种,D错误;答案选B。


科目:高中化学 来源: 题型:
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下。下列有关说法不正确的是( )

A. 制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO
B. 生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应
C. 粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D. 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的泄漏会造成严重的危险,以下说法有科学性错误的是
A. 由于大量苯溶入水中,渗入土壤,会对周边农田、水源造成严重的污染
B. 由于苯是一种易挥发、易燃的物质,周围地区如果有火星就可能引起爆炸
C. 可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D. 由于苯有毒,所有工作人员在处理事故时,都要做相关防护措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学让生活更美好。以下说法错误的是( )
A.酒精溶液可以使蛋白质变性,酒精纯度越高杀菌消毒效果越好
B.在烟花中加入某些金属元素,使焰火更加绚丽多彩
C.苏打水呈弱碱性,可以舒缓胃酸分泌过多时的不适感
D.在葡萄酒中添加微量二氧化硫作抗氧化剂,使酒保持良好品质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津港“8.12”特大火灾爆炸事故,造成了极其恶劣的社会影响。原因是化学危险 品随意堆放,管理人员安全意识淡漠,对人民的生命财产极不负责任。
下面是其中一部分危险品。请回答下列问题:
⑴ 写出过氧化氢的电子式
⑵ 上述危险品中,和水反应且符合下列条件的离子方程式
① 属于氧化还原反应 ② 水既不做氧化剂也不做还原剂
⑶ 4000C时,硝酸铵会发生爆炸,生成氮气、二氧化氮和水蒸气,20g硝酸铵爆炸放出QkJ的热量,试写出该反应的热化学方程式
⑷ 写出酸性高锰酸钾溶液与过氧化氢化应的离子方程式
⑸ 氰化钠有剧毒,为防止扩散,消防队员和工作人员离场前都用双氧水消毒。氰化钠和双氧水反应生成一种酸式盐和一种有刺激性气味的气体,反应的离子方程式是 ;调查查明现场有700吨的氰化钠,如果用密度为1.2g/mL质量分数为17%的双氧水进行消毒,最少需要这种双氧水_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用C、Fe和Al组成的混合物进行如图所示实物.
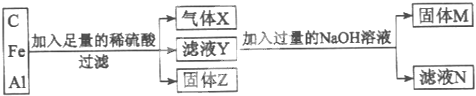
填写下列空白.
(1)气体X为 ,固体Z为 .
(2)滤液Y中除H+外,还含有的阳离子为 和 .
(3)滤液N中除Na2SO4和NaOH外,还含有的溶质为 (填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3: 物质结构与性质】
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
① Ti的基态原子价电子排布式为 。
② Fe的基态原子共有 种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3 CCl4==="2" KCl+2 CrO2Cl2+3 COCl2↑。
① 上述化学方程式中非金属元素电负性由大到小的顺序是 (用元素符号表示)。
② COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为 ,中心原子的杂化方式为 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm。则熔点:NiO (填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为 。
②已知该晶胞的摩尔质量为M g·mol-1,密度为d g·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是 cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511 pm,c=397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=![]() 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为 。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为:Mg17Al12 + 17H2=17MgH2 + 12Al。得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。
⑴ 熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是
⑵ 在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为
Ⅱ.某一反应体系有反应物和生成物共五种物质:
O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2―→O2
⑴ 该反应中的还原剂是
⑵ 该反应中,发生还原反应的过程是 →
⑶ 写出该反应的化学方程式,并标出电子转移的方向和数目 ;
⑷ 若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法错误的是( )
A.乙烯、苯都既能发生加成反应,也能被酸性高锰酸钾溶液氧化
B.塑料、合成橡胶和合成纤维都属于有机合成高分子化合物
C.淀粉、纤维素、油脂和蛋白质在一定条件下都能发生水解反应
D.C4H2Cl8有9种同分异构体(不含立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com