
分析 醋酸为弱酸,常温下,用0.1000mol/LCH3COOH溶液滴定NaOH溶液,当达到滴定终点时生成醋酸钠,醋酸根离子水解溶液显碱性,选择酚酞做指示剂,以此解答该题.
解答 解:常温下,用0.1000mol/LCH3COOH溶液滴定NaOH溶液,当达到滴定终点时生成醋酸钠,醋酸根离子水解溶液显碱性,当达到滴定终点时溶液的pH>7,溶液中各离子浓度从大到小的顺序为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),指示剂变色范围为:酚酞8-10,甲基橙为3.1-4.4,石蕊为5-8,为了减小滴定误差在滴定实验中使用的酸碱指示剂最好是酚酞,故选C,
故答案为:>;c(Na+)>c(CH3COO-)>c(OH-)>c(H+); C.
点评 本题考查弱电解质的电离和酸碱中和的定性判断,为高频考点,侧重考查学生的分析能力,注意把握离子浓度大小的比较以及酸碱指示剂的选择,难度不大.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:解答题
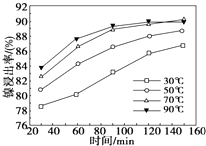 镍及其化合物具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.回答下列问题:
镍及其化合物具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原剂,脱除硝酸盐 | 向烧杯中加入① 碳粉,一段时间后,测定烧杯中NO3-的浓度 | NO3-浓度无明显变化,说明假设Ⅰ不成立 |
| 假设2:碳粉、铁粉形成无数个微小的原电池,促进了硝酸盐的脱除 | 按图示组装实验装置,一段时间后,测定NO3-浓度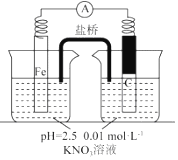 | ② Fe电极部分溶解,电流计指针偏转,说明假设2成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 诜项 | 实验操作 | 实验目的 |
| A | 将乙烯通入酸性KMnO4溶液中 | 证明乙烯能发生加成反应 |
| B | 向含酚酞的NaOH溶液中加入氯水 | 证明Cl2具有漂白性 |
| C | 常温下,向Fe和Cu中分别加入浓硝酸 | 比较Fe和Cu的金属活动性 |
| D | 将铁钉放入试管中,下端浸入食盐水中 | 验证铁的吸氧腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②④⑥ | C. | ②④ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
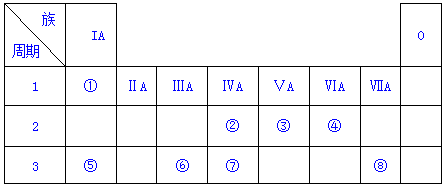
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: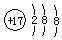 | B. | 甲烷分子的球棍模型: | ||
| C. | 氯化镁的电子式: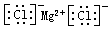 | D. | 原子核内有8个中子的氧原子:818O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com