
分析 (1)根据配制溶液的体积,常用容量瓶的规格选取对应的容量瓶;
(2)依据C=$\frac{1000ρω}{M}$计算浓盐酸的物质的量浓度;
(3)根据溶液稀释前后物质的量不变计算所需浓盐酸的体积,选择合适的量筒;
(4)根据配制一定物质的量浓度溶液的一般实验操作的步骤解答;
(5)根据c=$\frac{n}{V}$分析操作对溶质的物质的量或对溶液的体积的影响判断.
解答 解:(1)要配制盐酸220mL,则需要选择250ml的容量瓶,
故答案为:250;
(2)质量分数为36.5%的盐酸(密度为1.16g•cm-3)的浓盐酸的物质的量浓度C=$\frac{1000×1.16×36.5%}{36.5}$=11.6mol/L;
故答案为:11.6mol/L;
(3)设所需浓盐酸的体积为V,则有V×11.6mol/L=O.25L×1mol/L,得V=O.0216L,即21.6ml,应选择25ml的量筒,
故答案为:21.6; C;
(4)配制一定物质的量浓度溶液的一般实验操作的步骤:计算、量取、稀释、移液、洗涤、定容、摇匀,所以正确的顺序为:③①④②;
故答案为:③①④②;
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,导致量取浓盐酸中含有的氯化氢的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
若用干燥洁净的量筒量取浓盐酸时俯视,导致量取浓盐酸溶液 体积偏小,含有的氯化氢的物质的量偏小,溶液浓度偏低;
故答案为:偏低.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,明确配制过程是解题关键,题目难度不大.


 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题

| A. | 图I中,甲、乙的平衡常数分别为K1、K2,则K1=K2 | |
| B. | 图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低 | |
| C. | 图Ⅱ中,t时间是增大了压强 | |
| D. | 图Ⅲ是反应分别在甲、乙条件下达到平衡,说明甲温度高于乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Fe3++3OH-.
Fe3++3OH-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40gNaOH溶于1L水所得的溶液 | |
| B. | 将22.4LHCl溶于水配成1L溶液 | |
| C. | 1L含2mol K+的K2SO4溶液 | |
| D. | 将0.5mol•L-1的NaNO3溶液100mL加热蒸发掉50g水后的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol X、3mol Y | 2mol Z | 4mol Z |
| Z的浓度 (mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=Q | C. | 2p2<p3 | D. | α1+α3>1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)按已知的原子结构规律,27号元素在周期表中的位置是第四周期第Ⅷ族,其价电子的轨道排布图为
(1)按已知的原子结构规律,27号元素在周期表中的位置是第四周期第Ⅷ族,其价电子的轨道排布图为 .
. ),则配合物[Pt(en)2]Cl4中心离子的配位原子数为4.
),则配合物[Pt(en)2]Cl4中心离子的配位原子数为4. sp2
sp2 sp3
sp3

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
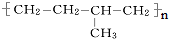 的单体的分子式为CH2=CH2 和CH2=CH-CH3
的单体的分子式为CH2=CH2 和CH2=CH-CH3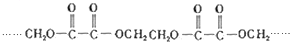 的单体的名称为HOOC-HOOC 和HOCH2-CH2OH.
的单体的名称为HOOC-HOOC 和HOCH2-CH2OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com