
����Ŀ��A��B��C��D��E��F��G��H��Ԫ�����ڱ�ǰ�����ڳ���Ԫ�أ���ԭ���������������������Ϣ���±���
Ԫ�� | �����Ϣ |
A | ԭ�Ӻ�����6�ֲ�ͬ�˶�״̬�ĵ��� |
C | ��̬ԭ����s����������p����������� |
D | ԭ�Ӱ뾶��ͬ����Ԫ������� |
E | ��̬ԭ�����������Ų�ʽΪ3s23p1 |
F | ��̬ԭ�ӵ������p������������ӵ������������������ӵ����������෴ |
G | ��̬ԭ�Ӻ�����7���ܼ���������ߵ��ܼ�����6������ |
H | ���ҹ�ʹ������ĺϽ��е�����ҪԪ�� |
���û�ѧ������գ�
(1) AԪ����Ԫ�����ڱ��е�λ��________��A��B��C����Ԫ�صĵ�һ�������ɴ�С������Ϊ_____����Ԫ�ط�����д����
(2) BԪ���������к�����ḻ��Ԫ���γɵ��������ķ��ӹ���Ϊ____��BԪ�����γɵĵ��ʷ�����������������Ŀ֮��Ϊ____��
(3) GԪ�صĵͼ������ӵ����ӽṹʾ��ͼ��________��FԪ��ԭ�ӵ���Χ�����Ų�ͼ��________��HԪ�صĻ�̬ԭ�Ӻ�������Ų�ʽ��________��
(4) DԪ�صĵ��ʼ��䳣�����������ɫ��Ӧ��Ҫ������ԭ�ӹ����е�______��A.ԭ�����չ���B.ԭ�ӷ�����ף�
(5) ����Ԫ������p������_______����Ԫ�ط�����д����
���𰸡��ڶ����ڵڢ�A�塡 I1(N)>I1(O)>I1(C)�� ������ 1:2 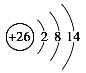
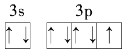 1s22s22p63s23p63d104s1��[Ar]3d104s1 B C��N��O��Al��Cl
1s22s22p63s23p63d104s1��[Ar]3d104s1 B C��N��O��Al��Cl
��������
�����ں����˶�״̬��ͬ����˺����м��ֲ�ͬ�˶�״̬�ĵ��ӣ�������м������ӣ���AΪC����̬ԭ��C��s����������p����������ȣ���ԭ��C�ĵ����Ų�ʽ����Ϊ1s22s22p4��Ҳ����Ϊ1s22s22p63s2��ͬ���ڴ�������ԭ�Ӱ뾶��������ԭ��D��ԭ�Ӱ뾶��ͬ����Ԫ�������DΪNa������Ԫ�ص�ԭ���������������Ƴ�CΪO��BΪN����̬ԭ��E���������Ų�ʽΪ3s23p1����EΪAl����̬Gԭ�Ӻ�����7���ܼ���������ߵ��ܼ�����6�����ӣ�GΪ26��Ԫ�أ���GΪFe��H���ҹ�ʹ������ĺϽ��е�����ҪԪ�أ��ҹ�ʹ����ߵĺϽ�����ͭ����HΪCu������Ԫ�ص�ԭ��������������̬ԭ��F�������p������������ӵ������������������ӵ����������෴���Ƴ�FΪCl���ݴ��жϡ�
�������Ϸ�����֪AΪC��BΪN��CΪO��DΪNa��EΪAl��FΪCl��GΪFe��HΪCu����
��1����������������AΪ̼Ԫ�أ�λ�����ڱ��ڶ�����IVA�壻ͬ���ڴ������ҵ�һ��������������A>��A����A>��A����C��N��O��һ�������ɴ�С��˳����N>O>C��
��2�������к�����ḻ��Ԫ����H��N��H�γ����������NH3������ӹ���Ϊ�����Σ�NԪ���γɵĵ���ΪN2��������ԭ��֮������������ɼ�ԭ�Ӽ�ֻ�γ�1���Ҽ���1molN2����1mol�Ҽ���2mol�м����Ҽ���м���Ŀ֮��Ϊ1��2��
��3��Fe�ĵͼ���������Fe2���������ӽṹʾ��ͼΪ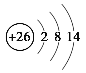 ��FԪ��ΪCl������Χ����Ϊ�������ӣ�����Χ�����Ų�ͼΪ
��FԪ��ΪCl������Χ����Ϊ�������ӣ�����Χ�����Ų�ͼΪ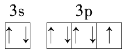 ��HԪ��ΪCu�����ڵ�������IB�壬��̬ԭ���Ų�ʽΪ1s22s22p63s23p63d104s1��[Ar]3d104s1��
��HԪ��ΪCu�����ڵ�������IB�壬��̬ԭ���Ų�ʽΪ1s22s22p63s23p63d104s1��[Ar]3d104s1��
��4����ɫ��Ӧ�ܹ������⣬�����ɫ��Ӧ��Ҫ������ԭ�ӹ����еķ�����ף���B��ȷ��
��5��p�������һ�����������p�ܼ��ϣ��������Ԫ������p������C��N��O��Al��Cl��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����㻯����A����ʽΪC9H10O2��B����Է���������A��79��J�����ᣬK�Ǿ�������ϩ���ĵ��壬G���Ȼ�����Һ�ܷ�����ɫ��Ӧ���ұ����ϵ�һԪȡ����ֻ�����֡�A��K֮��������ת����ϵ��
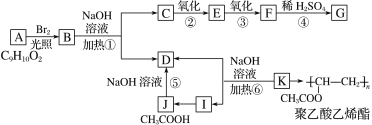
��֪���ٵ��ǻ���˫��̼ԭ������ʱ������ת����RCH==CHOH��RCH2CHO
����ONa���������ϲ��ᱻ������
��ش��������⣺
��1��������K�Ľṹ��ʽ��_______��I�й����ŵ�����Ϊ______��
��2����Ӧ�٢ܢݢ�������ˮ�ⷴӦ����___(�Ӧ���)����C��G����˳��Ϊ�ڢۢܣ�������ȡ�ܢڢۣ�ԭ����______��
��3��G������NaHCO3��Һ��Ӧ��1 molG��NaHCO3��Һ��Ӧʱ�������____molNaHCO3��
��4��д��B��C��D�Ļ�ѧ����ʽ_____________��
��5��ͬʱ��������Ҫ���A��ͬ���칹����________��(�����������칹)��
��.���б�������.�ܷ���������Ӧ��ˮ�ⷴӦ��
����Щͬ���칹���У���������������ͬ���칹��Ľṹ��ʽΪ________��
�ٺ˴Ź���������5�����շ壻��1mol��ͬ���칹��ֻ����1molNaOH��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���仯����㷺��������Ȼ�硣��ش��������⣺
��1�������ǵ�����̼Ԫ�ص�������ճء�
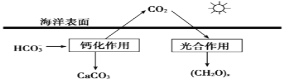
�����ں�ˮ�е�CO2��Ҫ��������̼��ʽ���ڣ�����CO2��H2CO3��___________��___________��
���ں���̼ѭ���У���ͨ������ͼ��ʾ��;����̼��д���ƻ����õ����ӷ���ʽ___________��
��2������CO2�ܽ��ں�ˮ��ʹ���ຣ���������پ���в���о������������ͼ��ʾ�����Ӻ�ˮ����ȡCO2�����Խ��ͻ�����������CO2�ĺ�����
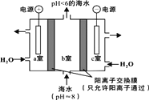
�� a�ҵĵ缫��Ӧʽ��__________��
�� ���ø�װ�ò���������X�ɴ���b���ų��ĺ�ˮ����ÿ��Żشĺϸ�ˮ��X�Ļ�ѧʽ��__________��
��3����֪��NH3��H2O��Kb=1.7��10��5��H2CO3��Ka1=4.3��10��7��Ka2=5.6��10��11����ҵ����β���е�CO2������֮һ�ǰ�ˮ��Һ���ռ��������������ǽ�������ȴ��15.5�桫26.5����ð�ˮ���չ�����CO2��������Һ��pH___________7�����������=������������������ȴ��15.5�桫26.5��Ŀ���ԭ����____________��
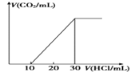
��4��Ϊ�˲���ij��ˮ����̼��������ȡ100mL��ˮ���ữ����N2����CO2������NaOH��Һ���ա�������Һ�еμ�1.0mol/L���ᣬ���ɵ�V(CO2)��V(����)�仯��ϵ��ͼ��ʾ����ԭ����Һ������Ũ���ɴ�С��˳��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���Ա�����������Ϊԭ�ϣ���ȡ�������������![]() ������֪�й����ʵķе������
������֪�й����ʵķе������

����ͼԲ����ƿ�м���12.2g�������30mL��������ܶ�ԼΪ0.79g/cm3������С�ļ���3mLŨ���ᣬ���Ⱥ��뼸�����Ƭ��С�ļ���30���ӣ�ʹ��Ӧ��֣��ñ�����������ֲ�Ʒ��
![]()
(1)�������Ƭ��������______������Ũ�����������_____��
(2)����Ӧ����ˮ��������ͬλ��18O��д���ܱ�ʾ��Ӧǰ��18Oλ�õĻ�ѧ��Ӧ����ʽ��_______��
(3)������������ֲ�Ʒ����������������������������ˮ�ȣ���������������ͼ���о��ƣ����������õ���һ����Ҫ����������_________�������ڵ�������__________��
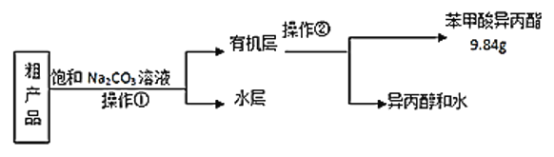
(4)�ڽ��в������ռ������������ʱӦ���Ƶ��¶ȷ�Χ_______��
A.80�桫100�� B.200�桫249�� C.217�桫219�� D.249������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������H2O2��������ṹ��������ԭ������һ����չ���������ҳֽ������ҳֽ��ļн�Ϊ94�㣬��ԭ������ļз�����O��H����O��O��֮��ļн�Ϊ97��������˵������ȷ����( )
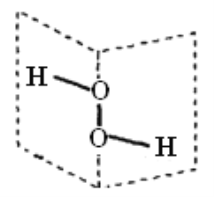
A. H2O2�����мȺ����Լ����ֺ��Ǽ��Լ�
B. H2O2Ϊ���Է���
C. H2O2�����е�����Oԭ�Ӿ���sp3�ӻ�
D. H2O2���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ(Cu3P2)������������ͭ������ͭ�Ǻ�����������ͭ�Ͻ���Ҫ������ĥ����͵���ԭ����
��1����̬ͭԭ�ӵĵ����Ų�ʽΪ_____�����̬ԭ�ӵļ۵����˶�״̬��___�֡���̬��ԭ�ӵ���Χ���ӹ����ʾʽ____
��2����ͭ��ˮ���ò����ж�������(PH3)������ӿռ乹��______��
��3������ͭ�е�����������Ԫ�ص縺�ԵĴ�СΪSn___P(����>����<����������)��
��4��ij����ͭ�����ṹ��ͼ��ʾ��
�����仯ѧʽΪ_______��
�ڸþ����о���Cuԭ�������Snԭ����___����
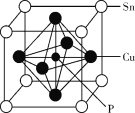
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ2A(g)��3B(g)![]() 4C(g)�����и����ݱ�ʾ��ͬ�����µĻ�ѧ��Ӧ���ʣ����з�Ӧ���е�������
4C(g)�����и����ݱ�ʾ��ͬ�����µĻ�ѧ��Ӧ���ʣ����з�Ӧ���е�������
A.��(C)��3.6mol/(L��min)B.��(B)��0.04mol/(L��s)
C.��(B)��0.9mol/(L��min)D.��(A)��1.6mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ʽ����ͼ������л���ɷ����ķ�Ӧ�����У� ��

��ȡ�� �ڼӳ� ����ȥ ������ ��ˮ�� ��������
A. �٢ڢۢݢ�B. �ڢۢܢݢ�
C. �٢ڢۢܢ�D. �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2SO3+I2+H2O=H2SO4+2HI����0.1molCl2ͨ��100ml�������ʵ�����HI��H2SO3�Ļ����Һ�У���һ���HI��������������˵����ȷ����
A�����ʵĻ�ԭ�ԣ�HI>H2SO3>HCl
B��HI��H2SO3�����ʵ���Ũ��Ϊ0.6 mol��L��1
C��ͨ��0.1molCl2������Ӧ�����ӷ���ʽΪ��5Cl2+4H2SO3+2I��+4H2O=4SO42��+I2+10Cl��+16H+
D������ͨ��0.05molCl2��ǡ���ܽ�HI��H2SO3��ȫ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com