
 )mol/L
)mol/L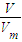 计算氨气的物质的量,再根据c=
计算氨气的物质的量,再根据c=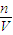 计算溶液的物质的量浓度;
计算溶液的物质的量浓度;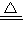 CuSO4+SO2↑+2H2O,64g铜的物质的量为1mol,硫酸的物质的量为0.1L×18mol/L=0.18mol,由方程式可知,硫酸不足量,且随反应进行浓硫酸变为稀硫酸,铜与稀硫酸不反应,实际反应的铜小于1mol;
CuSO4+SO2↑+2H2O,64g铜的物质的量为1mol,硫酸的物质的量为0.1L×18mol/L=0.18mol,由方程式可知,硫酸不足量,且随反应进行浓硫酸变为稀硫酸,铜与稀硫酸不反应,实际反应的铜小于1mol; =
=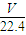 mol,氨水溶液的物质的量浓度为
mol,氨水溶液的物质的量浓度为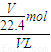 =
=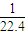 mol/L,故A正确;
mol/L,故A正确;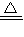 CuSO4+SO2↑+2H2O,64g铜的物质的量为1mol,硫酸的物质的量为0.1L×18mol/L=0.18mol,由方程式可知,硫酸不足量,且随反应进行浓硫酸变为稀硫酸,铜与稀硫酸不反应,故1mol铜不能完全反应,生成的SO2气体小于1mol,体积小于22.4L,故B错误;
CuSO4+SO2↑+2H2O,64g铜的物质的量为1mol,硫酸的物质的量为0.1L×18mol/L=0.18mol,由方程式可知,硫酸不足量,且随反应进行浓硫酸变为稀硫酸,铜与稀硫酸不反应,故1mol铜不能完全反应,生成的SO2气体小于1mol,体积小于22.4L,故B错误;

科目:高中化学 来源: 题型:
铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
|
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
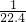 )mol/L
)mol/L查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量的浓度为(
| ||
| B.标准状况下,将64g 铜片投入到100ml 18 mol/L的浓硫酸中加热会产生22.4 L的SO2气体 | ||
| C.向1mol的碳酸钾固体中缓缓滴加少量的稀盐酸会产生1mol的CO2气体 | ||
| D.向含有1mol Ba(OH)2溶液中通入1molCO2气体就会产生1mol Ba(HCO3)2的白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com