
【题目】下列化学反应属于吸热反应的是( )
A.木炭燃烧
B.铝热反应
C.煅烧石灰石
D.氢氧化钠和硝酸反应
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体, D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。各物质之间的转换关系如下图,部分生成物省略。请回答下列问题:
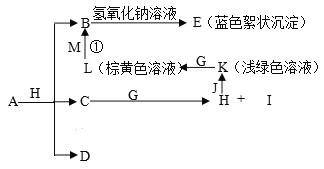
(1)写出A的化学式__________________,C的电子式______________________,
D的结构式______________________________。
(2)将22.4L(标准状况)D气体通入1L 1mol/L NaOH溶液中,完全吸收后,溶液中除了Na+外,还大量存在的离子是______________________________。
(3)已知M溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的离子方程式___________________________________________________________。
(4)检验化合物K中阳离子的实验方法是______________________________________
(5)写出反应K+G→L的化学方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.32 g O2占有的体积约为22.4 L
B.22.4 L N2含阿伏加德罗常数个氮分子
C.在标准状况下,22.4 L水的质量约为18 g
D.22 g二氧化碳与标准状况下11.2 L HCl约含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,氢氧化钙固体在水溶液中达到溶解平衡:Ca(OH)2 (s) ![]() Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
A. CH3COONa B. AlCl3 C. NaOH D. CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D是中学化学常见的混合物分离或提纯的基本装置。
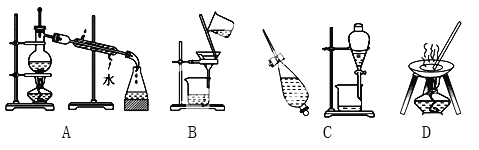
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪一种装置,将A、B、C、D填入适当的空格中。
(1)从碘水中提取碘_____________________________;
(2)实验室制取蒸馏水_____________________________;
(3)去粗盐中的泥沙_____________________________;
(4)与海水晒盐原理相符的是___________________________。
Ⅱ.现有下列八种物质:①HCl气体②Cu ③CO ④CO2 ⑤金刚石 ⑥KMnO4固体 ⑦Ba(OH)2溶液 ⑧熔融KAl(SO4)2
(1)属于单质的是_________;属于酸性氧化物的是_________;所给状态能导电的电解质是_________;(填所给物质的序号)
(2)写出Ba(OH)2在水中的电离方程式:____________________________________________;
(3)用双线桥表示该反应中电子转移的方向和数目_______
2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
若有0.8mol还原剂被氧化,则转移电子的物质的量是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化物是一类重要的化工原料,具有广泛的用途。完成下列填空:
(1)Na2S溶液中,水的电离程度会_________(填“增大”、 “减小”或“不变”);微热该溶液, pH 会_________(填“增大”、 “减小”或“不变”)。
(2)Na2S 溶液中各离子浓度由大到小的顺序为: ___________________________________。
(3)向 Na2S 和 Na2SO3 的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
__ Na2S+ __ Na2SO3+__ H2SO4→__ Na2SO4+__ S↓+ __ H2O
①配平上述化学方程式,标出电子转移的方向和数目______。
②反应中被氧化的元素是______________。
(4)CuS和FeS都是难溶于水的固体,工业上可用 FeS 将废水中的 Cu2+转化为CuS除去,请结合相关原理进行解释:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中含有的中哑铃形C ![]() 的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( )
的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( ) 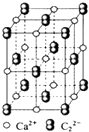
A.1个Ca2+周围距离最近且等距离的C22﹣数目为6
B.该晶体中的阴离子与F2是等电子体
C.6.4克CaC2晶体中含阴离子0.1mol
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氢化钠(NaH) 是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。根据信息完成下列各空:
(1)氢化钠的电子式为_____________________________。
(2)氢化钠与水反应的化学方程式为_____________________,反应的氧化剂为___________。该反应过程中,被破坏的化学键有_____________(填序号,下同),形成的化学键有______________。
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系: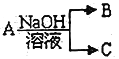 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。
(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为________________________________________________;
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为_____________________________;A 最高价氧化物的水化物与NaOH 溶液反应的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素V、W、X、Y、Z的原子序数依次增大。由这五种元素组成的九种物质中,n、r、u是气体单质,其余均为化合物;n是黄绿色气体,m是能使湿润的红色石蕊试纸变蓝的无色气体,p是无色液体,q是淡黄色固体。它们的转化关系如图所示。
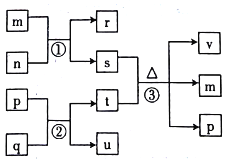
下列说法正确的是
A. 实验室制取m和u时,气体发生装置可以相同
B. 原子半径:W>X>Y
C. 反应①、②均为置换反应
D. n与t溶液反应时,t作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com