
摩托罗拉公司研发了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应式为2CH3OH+3O2+4OH-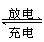 2CO
2CO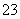 +6H2O,则下列有关说法错误的是( )
+6H2O,则下列有关说法错误的是( )
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应式为CH3OH-6e-+8OH-===CO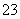 +6H2O
+6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
Ⅰ.2008年5月12日汶川大地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上制取漂白粉的化学方程式为______________________________________。
(2)漂白粉的有效成分是(填化学式)_______________________________。
(3)漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸。化学反应方程式为________________________________________________________________________
________________________________________________________________________。
Ⅱ.钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术。其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃。其过程可以用如下方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O===3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
则反应②中的氧化剂是________(填化学式),整个过程中,每有168 g Fe参加反应,则转移________ mol 电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下:
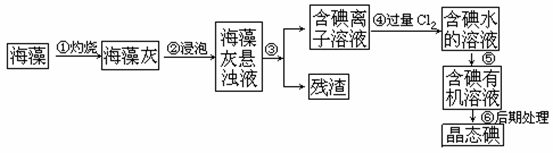
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③________,步骤⑤_______。
(2)写出步骤④对应反应的离子方程式:____________________ __。
(3)提取碘的过程中,可供选择的有机试剂是_______________。
A. 酒精 B. 醋酸 C. 四氯化碳 D. 苯
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是____________________________________。
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。
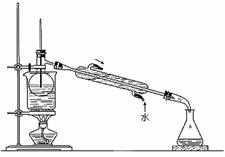
查看答案和解析>>
科目:高中化学 来源: 题型:
用洁净的铂丝蘸取某种无色溶液,在无色火焰上灼烧,火焰呈黄色,说明该溶液中( )
A.只有Na+ B.可能有Na+,可能有K+
C.一定有K+ D.一定有Na+,也可能有K+
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐是人类生活中不可缺少的物质,海水中含有大量食盐。
某地出产的粗盐中,所含杂质是CaCl2,通过下面的实验可制得纯净的NaCl2。
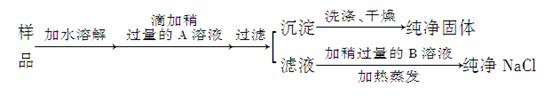 请回答:
请回答:
(1)加入的A是__________,检验A已过量的方法是_________________________
________________________________________________________________________。
(2)加入的B是__________,加入稍过量B的目的是________________________。
(3)为检验沉淀是否洗净,最好在最后几滴洗出液中加入______________________溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,通电5 min后,电极5的质量增加了2.16 g,回答:
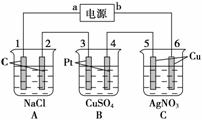
(1)电源:a是________极,C池是________池。
A池阳极电极反应式为__________________,阴极电极反应式为__________________。C池阳极电极反应式__________________,阴极电极反应式为
________________________________________________________________________。
(2)如果B槽中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
________________________________________________________________________。
(3)如果A池溶液也是200 mL(电解过程中溶液体积不变),则通电后,溶液的pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用低温技术可处理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:
4NH3(g)+6NO(g)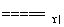 5N2(g)+6H2O(l)
5N2(g)+6H2O(l)
ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是 ( )。
A.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中NO的转化率减小
C.单位时间内生成NH3和H2O的物质的量之比为2∶3时,反应达到平衡
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要
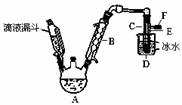 加热,图中省去了加热装置。有关数据见表:
加热,图中省去了加热装置。有关数据见表:
表.乙醇、溴乙烷、溴有关参数
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
⑴ 制备操作中,加入的浓硫酸必需进行稀释,其目的是 (选填序号)。
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.减少HBr的挥发d.水是反应的催化剂
⑵ 已知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应
的化学方程式 。
⑶ 仪器B的名称 ,冷却水应从B的 (填“上”或“下”)口流进。
⑷ 反应生成的溴乙烷应在 中(填“A”或“C”中)。
⑸ 若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列 (选填序号)
溶液来洗涤产品。
a.氢氧化钠 b.亚硫酸钠 c.碘化亚铁 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
.某学习兴趣小组讨论辨析以下说法,其中说法正确的是( )
①通过化学变化可以实现16O与18O间的相互转化
②灼烧钠的化合物时,火焰呈黄色,发生化学反应
③碱性氧化物一定是金属氧化物
④只由一种元素组成的物质一定为纯净物
⑤石墨和C60是同素异形体
⑥糖类、蛋白质、油脂属于天然高分子化合物
A.③⑤⑥ B.①② C.③⑤ D.①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com