
Q、R、T、X、Y、Z是六种原子序数依次增大的前四周期常见元素,其相关信息如下表:
元素 | 相关信息 |
Q | Q的单质是实验室常用的惰性电极材料 |
R | R原子基态时2p原子轨道上有3个未成对电子 |
T | 负二价的元素T的氢化物在通常状况下是一种液体,且其中T的质量分数为88.9% |
X | X是第三周期电负性最大的元素 |
Y | 元素Y位于周期表的第10列 |
Z | Z存在质量数为65,中子数为36的核素 |
(1)Z元素的原子基态时的电子排布式是________。
(2)下列叙述正确的是________(填字母序号)。
a.Q的气态氢化物比R的气态氢化物稳定
b.Q的含氧酸一定比R的含氧酸酸性强
c.R的气态氢化物的熔点在同族元素的氢化物中最低
d.R的第一电离能、电负性都比Q的大
(3)Q和T可形成两种常见化合物,分别表示为QT和QT2。QT分子中σ键和π键的个数比为________;QT2分子中,Q原子采取________杂化。
(4)笑气(R2T)是一种麻醉剂,有关理论认为R2T与QT2分子具有相似的结构。故R2T的空间构型是________,其为________(填“极性”或“非极性”)分子。
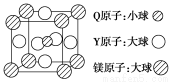
(5)含有Q、Y和镁三种元素的某种晶体具有超导性,其结构如图所示。则该晶体的化学式为________;晶体中每个镁原子周围距离相等且最近的Y原子有______个。
(1)1s22s22p63s23p63d104s1(或[Ar]3d104s1)
(2)d (3)1∶2 sp (4)直线形 非极性
(5)MgNi3C 12
【解析】Q的单质是实验室常用的惰性电极材料,则Q是C元素;R原子基态时2p原子轨道上有3个未成对电子,故R为N元素;根据氢化物的化学式H2T知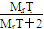 ×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。
×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。


科目:高中化学 来源:2014年高考化学指导冲关 第14练有机物的组成、结构和性质练习卷(解析版) 题型:选择题
核糖是合成核酸的重要原料,结构简式为CH2OH—CHOH—CHOH—CHOH—CHO。下列关于核糖的叙述正确的是( )
A.与葡萄糖互为同分异构体
B.可以与银氨溶液作用形成银镜
C.可以跟氯化铁溶液作用显色
D.可以使紫色石蕊试液变红
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第10练常见有机化合物及其应用练习卷(解析版) 题型:选择题
某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示。请根据其结构特点判断下列有关说法中正确的是( )
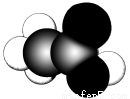
①该有机物的化学式为C2H4O2 ②该有机物的水溶液呈酸性且酸性比碳酸强 ③该有机物能发生酯化反应
A.全部正确 B.只有②错误 C.只有③ D.全部错误
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(二) (解析版) 题型:填空题
某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
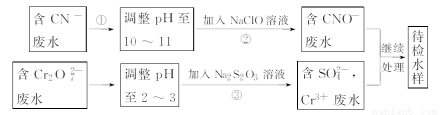
回答下列问题:
(1)上述处理废水流程中主要采用的方法是_____________。
(2)流程②中,反应后无气体放出,该反应的离子方程式为_______。
(3)含Cr3+废水需进一步处理,请你设计一个处理方案:_______。
(4)反应③中,每消耗0.4 mol Cr2O72-转移2.4 mol e-,该反应离子方程式为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(二) (解析版) 题型:选择题
工业上可用硫酸铝与硫黄焙烧制备氧化铝:2Al2(SO4)3+3S  2Al2O3+9SO2↑,下列有关说法中正确的是( )
2Al2O3+9SO2↑,下列有关说法中正确的是( )
A.反应中Al2(SO4)3被氧化
B.Al2(SO4)3、Al2O3均含有离子键和共价键
C.5.1 g Al2O3含有9.03×1022个阴离子
D.该反应中,每转移0.3 mol电子生成5.04 L SO2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(三) (解析版) 题型:选择题
绿原酸的结构简式如图所示下列有关绿原酸的说法不正确的是( )
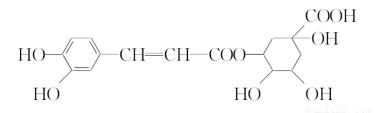
A.分子式为C16H18O9
B.能与Na2CO3反应
C.能发生取代反应和消去反应
D.0.1 mol绿原酸最多与0.8 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(一) (解析版) 题型:填空题
已知:A、B、C、D为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;D的基态原子的M电子层上有4个未成对电子。
请回答下列问题:
(1)D是元素周期表中第________周期,第________族的元素;其基态原子的外围电子排布式为________。
(2)A、B、C、D四种元素中,电负性最大的是________(填元素符号)。
(3)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为________。B的氢化物的沸点远高于A的氢化物的沸点的主要原因是________________________________________________________________。
(4)D能与AC分子形成D(AC)5,其原因是AC分子中含有________________。D(AC)5常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断D(AC)5晶体属于________(填晶体类型)。
(5)SiO2的晶胞可作如下推导:先将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成Si原子,再在每两个不共面的“小立方体”中心处各放置一个Si原子便构成了晶体Si的一个晶胞。再在每两个相邻的Si原子(距离最近的两个Si原子)中心连线的中点处增添一个O原子,便构成了SiO2晶胞,故SiO2晶胞中有________个Si原子,________个O原子。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练4 化学实验练习卷(解析版) 题型:选择题
已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
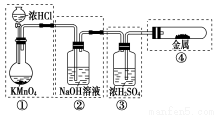
A.①② B.② C.②③ D.②③④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练1 化学基本概念练习卷(解析版) 题型:填空题
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。

提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com