
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。(B中装的是无水硫酸铜)
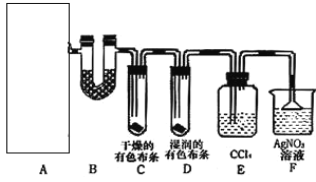
(1)A是氯气发生装置,实验室制取Cl2的原理是_____(用离子方程式表示)
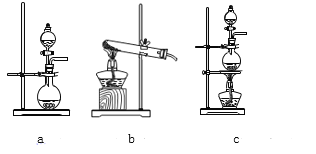
(2)该实验中A部分的装置是_____(填字母)
(3)若用含有0.2molHCl的浓盐酸与足量的氧化剂反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是(填序号)_____
A.浓盐酸的浓度随着反应的进行变稀以后,将不再反应
B.加热时浓盐酸因挥发而损失
C.氧化剂不足
(4)装置E的作用是______。
(5)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。该装置中应放入_______试剂。
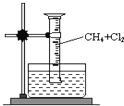
(6)用如图所示装置,收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
①该反应的反应类型为_________;
②该反应的化学方程式为________;(只写第一步)
【答案】MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O c AB 吸收氯气 湿润的淀粉KI试纸(或湿润的有色布条) 取代反应 CH4+Cl2
Mn2++Cl2↑+2H2O c AB 吸收氯气 湿润的淀粉KI试纸(或湿润的有色布条) 取代反应 CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
【解析】
本题以氯气为载体,综合考查常见的基本实验操作、氯气的性质检验以及尾气处理等。注意紧扣实验目的“探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质”解答。
(1)实验室制取氯气一般用二氧化锰氧化浓盐酸生成,方程式为MnO2+4HCl![]() MnCl2+Cl2↑+H2O,离子方程式为MnO2+4H++2Cl-
MnCl2+Cl2↑+H2O,离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)该实验中A部分的装置是固液加热型,故答案选c;
(3)A.随着反应的进行盐酸的浓度会逐渐降低,而二氧化锰是不能氧化稀盐酸的,所以实际生成的氯气总是小于理论值,故A正确;
B.加热时浓盐酸因挥发而损失,还原剂减少,所以实际生成的氯气总是小于理论值,故B正确;
C.0.2molHCl的浓盐酸与足量的氧化剂反应,故C错误;
答案选AB;
(4)由于F是用来检验氯化氢的,而氯气也能和硝酸银反应产生白色沉淀,所以在通入硝酸银溶液之前要先除去氯气。利用氯气能溶解的有机溶剂中,装置E的作用是除去氯气;
(5)氯气能溶解在四氯化碳中,但无法确定是否完全被吸收。所以需要在E和F之间连接1个装置,用来检验氯气是否完全被除去。可利用氯气的氧化性,能把碘化钾氧化生成单质碘,而单质碘能和淀粉发生显色反应,使溶液显蓝色。所以试剂是湿润的淀粉KI试纸。也可以通过漂白性来检验,因此也可以选择湿润的有色布条;
(6)①甲烷和氯气发生反应,甲烷分子中的氢原子被氯原子取代,所以属于取代反应;
②甲烷与氯气在光照下发生取代反应,甲烷分子中的氢原子被氯气分子中的氯原子取代,生成一氯甲烷和氯化氢,该反应的化学方程式为CH4+Cl2![]() CH3Cl+HCl。
CH3Cl+HCl。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】金属钠是体心立方堆积,关于钠晶体,下列判断合理的是 ( )
A. 其熔点比金属铝的熔点高
B. 一个钠的晶胞中,平均含有4个钠原子
C. 该晶体中的自由电子在外加电场作用下可发生定向移动
D. 该晶体中的钠离子在外加电场作用下可发生定向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列物质中:
(1)互为同分异构体的有_______ (2)互为同素异形体的有_______
(3)属于同位素的有__________ (4)属于同一种物质的有______。(填序号)
①液氯和氯气 ②白磷和红磷 ③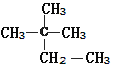 和
和![]() ④3717Cl和3517Cl⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥
④3717Cl和3517Cl⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥![]() 和
和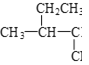 ⑦CH4和CH3CH2CH3
⑦CH4和CH3CH2CH3
Ⅱ.现有6种物质:①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_______。
(2)含共价键的离子化合物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
A. 1mol NH3所含有的原子数为NA
B. 常温常压下,22.4L氧气所含的原子数为2NA
C. 常温常压下,48g O3所含的氧原子数为3NA
D. 1 L 0.1mol/LNaCl溶液中所含的Na+为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3S +6KOH=K2SO3 +2K2S +3H2O 中,作还原剂和作氧化剂的硫原子个数比为
A.1:2 B.2:1 C.1:1 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) (单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) (单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
A. 4v(NH3)=5 v(O2)B. 5 v(O2)=6 v(H2O)
C. 2v(NH3)=3 v(H2O)D. 4v(O2)=5 v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1。已知:Mg与Br2反应剧烈放热;MgBr2具有强吸水性。下列说法错误的是( )
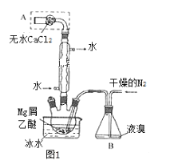
A. 实验必须要缓慢通入干燥的N2以免反应过于剧烈
B. 若用干燥的空气代替干燥的N2,其主要的缺点是制得的MgBr2中含有杂质。
C. 装有无水CaCl2固体A的作用是防止外界水蒸气进入反应装置
D. 冷凝管起冷凝回流作用,可防止乙醚、溴等的挥发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com